2007年11月,我国自行研制的长征三号甲运载火箭载着“嫦娥一号”探测器升空,成功实现了绕月飞行.第一、二级火箭使用的推进剂是液态偏二甲肼和四氧化二氮.已知偏二甲肼含C、H、N三种元素,其中C、N两元素的质量分数分别为40.0% 和46.7%,在气态时,偏二甲肼的密度是相同条件下H
2密度的30倍.请填写下列空白:
(1)偏二甲肼的分子式为
C2H8N2
C2H8N2
;若0.2mol液态偏二甲肼与液态N
2O
4完全反应,生成气态的N
2、H
2O和CO
2,同时放出510kJ热量,试写出该反应的热化学方程式:
C2H8N2(1)+2N2O4(1)═2CO2(g)+4H2O(g)+3N2(g);△H=-2550kJ?mol-1
C2H8N2(1)+2N2O4(1)═2CO2(g)+4H2O(g)+3N2(g);△H=-2550kJ?mol-1
(2)满足偏二甲肼分子式的同分异构体有
6
6
种.写出符合分子中含两个甲基的结构简式:
CH3-NH-NH-CH3、NH2-N(CH3)2
CH3-NH-NH-CH3、NH2-N(CH3)2
.
(3)肼(N
2H
4)又称联氨,是一种可燃性液体,也可用作火箭燃料.肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30% 的KOH溶液,放电时生成氮气和水,则肼-空气燃料电池放电时,负极的电极反应式是
N2H4+4OH--4e-═N2+4H2O
N2H4+4OH--4e-═N2+4H2O
.
(4)肼可看作是氨分子内的一个氢原子被氨基取代的衍生物,肼的水溶液呈弱碱性,是因为溶液中存在平衡:H
2N-NH
2+H
2O

H2N-NH3++OH-(或N2H3++OH-)
H2N-NH3++OH-(或N2H3++OH-)
.

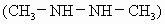 完全燃烧,放出50kJ热量,则二甲基肼的燃烧热为
完全燃烧,放出50kJ热量,则二甲基肼的燃烧热为