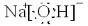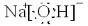(2012?河北区一模)短周期中的A、B、C、D、E五种元素,原子序数依次增大,A、D同主族;A、B的原子序数之和等于C的原子序数;C
2-离子与D
+离子的核外电子数相等;B原子与D
+离子的核外电子数之和等于E原子的核外电子数,且D、E两元素能形成微粒个数比为1:1的离子化合物.
(1)E元素的离子结构示意图为
.
(2)A与B元素、A与C元素均可构成18电子的分子,其化学式分别为
N2H4
N2H4
、
H2O2
H2O2
.
(3)A、B、C、D中的任意三种元素可组成多种化合物,X和Y是其中的两种.X和Y都是既含离子键又含共价键的离子化合物;将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的pH<7,Y水溶液的pH>7.将0.2mol/L的X溶液与0.1mol/L的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为
NH4NO3
NH4NO3
,Y的化学式为
NaOH
NaOH
;
②混合溶液中各种带电微粒的物质的量浓度由大到小的顺序为
c(NO3-)>c(NH4+)>c(Na+ )>c(OH-)>c(H+)
c(NO3-)>c(NH4+)>c(Na+ )>c(OH-)>c(H+)
.
(4)在10L的密闭容器中,通入1mol B
2气体和3mol A
2气体,一定温度下反应生成BA
3气体,当反应达到平衡时,B
2的浓度为0.01mol/L,同时放出约83.2kJ的热量,该反应的热化学方程式为
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
.