
题目列表(包括答案和解析)
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示,已知这个反应速率随着溶液中c(H+)增大而加快。

(1)反应开始时反应速率加快的原因是_______________________________________。
(2)反应后期反应速率下降的原因是_________________________________________。
(3)若纵坐标表示的某一反应物的单位时间内的浓度变化,图中阴影部分的“面积”表示_________________________ _______________。
(1)请在流程中的( )中写上合适的试剂,在[ ]中写上实验操作名称。?
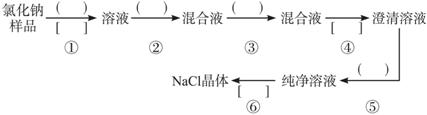
(2)写出有关反应的化学方程式:?
第②步________________?
第③步________________?
第⑤步________________?
(2)近年来医学界发现,铝对人体健康危害性很大,能引起痴呆、骨痛、贫血、甲状腺功能降低、胃液分泌减少等多种疾病。为了防止铝对人体的慢性中毒,不要用铝锅来烹调酸、碱性强的食品,原因是____________。
A.Ag+的浓度不再改变
B.Ag+的生成速率和Ag+、Cl-结合生成AgCl的速率相等
C.AgCl的质量不再减少
D.Ag+与Cl-的物质的量比为1∶1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com