
题目列表(包括答案和解析)
(10分)如图为相互串联的甲、乙两电解池,试回答:
(1)甲池若为用电解原理精炼铜的装置,则:
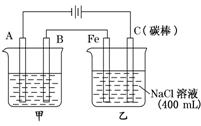
A是________极,材料是________,电极反应为___________;
B是________极,材料是_____ _,主要电极反应为________,
电解质溶液为________.
(2)乙池中若滴入少量酚酞试液,电解一段时间后Fe电极附近呈________色.
(3)若甲池中阴极增重12.8g,则乙池中阳极放出的气体在标准状况下的体积为______L.若此时乙池剩余液体为400 mL,则电解后溶液的pH为________.
(14分) 硫酸是工业生产中一种重要的化工产品,我国工业生产硫酸的主要方法是接触法,主要原料为黄铁矿,请回答下列问题:
(1)已知煅烧黄铁矿的化学方程式为 4FeS2 + 11O2  2Fe2O3
+ 8SO2
2Fe2O3
+ 8SO2
该反应中氧化剂和氧化产物之比为 ;标准状态下得到4.48升SO2 时,一共转移了 mol e- 。(每空3分)
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:根据上表回答,SO2转化到SO3的
最佳反应条件是 。(每空2分)
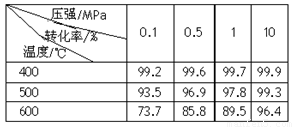
A.400-500℃ 0.1 MPa B.400℃ 10 MPa
C.500℃ 10 MPa D.400-500℃ 1 MPa
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 KJ,写出该反应的热化学方程式: 。若在该条件下将2 mol SO2 放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 KJ,则此时SO2的转化率为 (用含Q1、Q2代数式表示)。(每空2分)
(4)市售浓硫酸的密度是1.84 g / cm3、质量分数为98 % ,若用H2SO4· XH2O来表示这种浓硫酸,则X为 。(每空2分)
(满分10分)有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变。起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等。在400℃条件下,发生如下反应:2SO2(g) + O2(g) 2SO3(g)。
2SO3(g)。
(1)达到平衡时,所需的时间t(A) t(B),A容器中SO2的转化率比B容器中 。(填“大、小或相等)
(2)达到(1)所述平衡后,若向两容器中通入少量的等量氩气,A容器中化学平衡 移动,B容器中化学平衡 移动。(填“向左、向右、不”)
(3)达到(1)所述平衡后,若向两容器中通入等量原反应气体,再达到平衡时,A容器中c(SO3) ,B容器中SO3的质量分数 。(填“增大、减少或不变”)
(共10分)甲醇合成反应及其能量变化如图所示:
(1)写出合成甲醇的热化学方程式________________________________。
实验室在1 L的密闭容器中进行模拟合成实验。将1 mol CO和2 mol H2通入容器中,分别恒温在300 ℃和500 ℃反应,每隔一段时间测得容器内CH3OH的浓度如下表所示:
| 时间浓度(mol/L)温度 | 10 min | 20 min | 30 min | 40 min | 50 min | 60 min |
| 300 ℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500 ℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
( 10分)低碳经济呼唤新能源和清洁环保能源。煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题。已知:CO(g) + H2O(g) H2(g) + CO2(g) △H= a kJ·mol-1 的平衡常数随温度的变化如下表:
H2(g) + CO2(g) △H= a kJ·mol-1 的平衡常数随温度的变化如下表:
|
温度/℃ |
400 |
500 |
850 |
|
平衡常数 |
9.94 |
9 |
1 |
(1)上述正反应方向是 反应(填“放热”或“吸热”)。
t1℃时物质浓度(mol/L)的变化

|
时间(min) |
CO |
H2O |
CO2 |
H2 |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
|
5 |
0.116 |
0.216 |
0.084 |
|
|
6 |
0.096 |
0.266 |
0.104 |
|
(2) t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。①与2min时相比,3min时密闭容器中混合气体的平均摩尔质量 (填增大、减小或不变)。
②表中3 min~4 min之间反应处于 状态;CO的体积分数 16% (填大于、小于或等于)。
③反应在4 min~5 min,平衡向逆方向移动,可能的原因是____(单选),表中5 min~6 min之间数值发生变化,可能的原因是______(单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
(3)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com