
题目列表(包括答案和解析)
(共10分)二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用焦炭与水蒸气在高温下的反应产物(水煤气)合成二甲醚。请回答下列问题:
(1)、制水煤气的主要化学反应方程式为: 。
(2)、煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为: 。
(3)、利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) CO(g)
CO(g) CH3OH(g)
CH3OH(g) 90.8 kJ
90.8 kJ
② 2CH3OH(g) CH3OCH3(g)
CH3OCH3(g) H2O(g)
H2O(g) 23.5 kJ
23.5 kJ
③ CO(g) H2O(g)
H2O(g) CO2(g)
CO2(g) H2(g)
H2(g) 41.3 kJ
41.3 kJ
总反应:3H2(g) 3CO(g)
3CO(g) CH3OCH3(g)
CH3OCH3(g) CO2(g)
CO2(g) Q,其中Q
Q,其中Q kJ;
kJ;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
(填字母代号)。
a.低温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度
(4)、已知某温度下反应②2CH3OH(g) CH3OCH3(g)
CH3OCH3(g) H2O(g)在一密闭容器中进行到10min时恰好达平衡,测得各组分的浓度如下:
H2O(g)在一密闭容器中进行到10min时恰好达平衡,测得各组分的浓度如下:
|
物质 |
CH3OH |
CH3OCH3 |
H2O |
|
浓度/(mol·L |
0.44 |
0.6 |
0.6 |
比较此时正、逆反应速率数值(单位相同)的大小: (甲醇)
(甲醇)  (水)(填“>”、“<”或“=”)。
(水)(填“>”、“<”或“=”)。
反应开始时 (CH3OH)
(CH3OH) ;
;
该时间内的平均反应速率 (CH3OH)
(CH3OH) ;
;
该温度下反应的平衡常数值为 。(精确到0.01)
(12分)(1)“嫦娥一号”登月成功,实现了中国人“奔月”的梦想.“嫦娥一号”使用的推进剂是液氢和液氧,这种推进剂的优点是相同质量时,氢气放出的热量多,产物为水无污染。
已知:H2(g)+O2(g)=H2O(l) ΔH=-285.8 kJ/mol ; H2(g)=H2(l) ΔH=-0.92 kJ/mol
O2(g)=O2(l) ΔH=-6.84 kJ/mol ; H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
请写出液氢和液氧生成气态水的热化学方程式:_______________________________.
(2)已知:①NH3(g)+HCl(g)===NH4Cl(s) ΔH=-176 kJ/mol
②NH3(g)+H2O(l)===NH3·H2O(aq) ΔH =-35.1 kJ/mol
③HCl(g)===HCl(aq) ΔH = -72.3 kJ/mol
④NH3·H2O(aq)+HCl(aq)===NH4Cl(aq)+H2O(l) ΔH=-52.3 kJ/mol
则NH4Cl(s)===NH4Cl(aq)的ΔH=______
(3)分别取40 mL的0.50 mol/L盐酸与0.55 mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
① 理论上稀强酸、稀强碱反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式 __
② 假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容
c=4.18 J/(g·℃).为了计算中和热,实验时还需测量的数据有(填序号)__________;
A.反应前盐酸溶液的温度 B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度 D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度 F.反应后混合溶液的质量
③ 某学生实验记录数据如下:
|
实验 序号 |
起始温度t1/℃ |
终止温度t2/℃ |
|
|
盐酸 |
氢氧化钠 |
混合溶液 |
|
|
1 |
20.0 |
20.1 |
23.2 |
|
2 |
20.2 |
20.4 |
23.4 |
|
3 |
20.5 |
20.6 |
23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=__________ __;
④假定该学生的操作完全同上,实验中改用100 mL 0.5 mol/L盐酸跟100 mL 0.55 mol/L氢氧化钠溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”).
下面是四种盐在不同温度下的溶解度(g/100 g H2O):
NaNO3 KNO3 NaCl KCl
10℃ 80.5 20.9 35.7 31.0
100℃ 175 246 39.1 56.6
(计算时假定:①盐类共存时不影响各自的溶解度;②过滤晶体时,溶剂损耗忽略不计)
(1)取23.4 g NaCl和40.4 g KNO3,加70.0 g H2O,加热溶解。在100℃时蒸发掉 50.0 g H2O,维持该温度,过滤析出晶体,计算所得晶体的质量(m高温)。
将滤液冷却至10 ℃,待充分结晶后过滤。计算所得晶体的质量(m低温)。
(2)另取34.0gNaNO3和29.8 g KCl,同样进行如上实验。10℃时析出的晶体是_______________(写化学式)。100℃和10℃得到的晶体质量(m′高温和m′低温)分别是多少?
将MgCl2溶液加入NaOH和Na2CO3的混合溶液中,溶液中的离子反应如下:先发生Mg2++2OH-===Mg(OH)2↓,后发生Mg2++CO![]() ===MgCO3↓;经查溶解度表得知, Mg(OH)2的溶解度小于MgCO3的溶解度。在溶解度表中有这样一组数据,表示四种物质在水中、液氨中的溶解度(g溶质/100 g溶剂),如下表:
===MgCO3↓;经查溶解度表得知, Mg(OH)2的溶解度小于MgCO3的溶解度。在溶解度表中有这样一组数据,表示四种物质在水中、液氨中的溶解度(g溶质/100 g溶剂),如下表:
| 溶质 溶剂 | AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
| 水 | 170 | 9.3 | 1.5×10-4 | 33.3 |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
(1)分别是1.0 mol· L-1的Ag+、Ba2+、NO![]() 和Cl-在水中发生反应的离子方程式是______________________________________________________________。
和Cl-在水中发生反应的离子方程式是______________________________________________________________。
(2)分别是0.50 mol· L-1的以上四种离子在液氨中发生反应的离子方程式是__________________________________________________。
II(6分)、某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有
 Fe3+、Ba2+、K+、OH-、NO3-、
Fe3+、Ba2+、K+、OH-、NO3-、![]() 、
、![]() 。为了进一步确认,对该溶液进行实验检测:
。为了进一步确认,对该溶液进行实验检测:
①仔细观察,该溶液呈无色、透明、均一状态。
②向100mL溶液中滴入稀硫酸,有23.3g白色沉淀产生,再加稀硝酸,白色沉淀不消失。回答下列问题:由此可知,除了含有Na+、Mg2+、Cl-外,该溶液中肯定还含有的离子及其物质的量浓度为___________,肯定没有的离子是___________,可能含有的离子是___________。
III(6分).试样X由氧化亚铁和氧化铜组成。取质量相等的两份试样进行下图所示实验:

(1)写出步骤③发生的全部反应的离子方程式。
(2)若Y和Z充分反应,生成的不溶物的质量是m,则每份试样X中氧化铜的质量为 (用m表示)。
鸦片最早用于药物(有止痛、止泻、止咳的作用),长期服用会成瘾,使人体质衰弱,精神颓废,寿命缩短。鸦片具有复杂的组成,其中的罂粟碱的分子结构如右图:已知该物质的燃烧产物为
CO2、H2O和N2,1mol该化和物完全燃烧消耗的O2的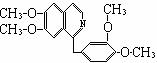
物质的量及在一定条件下与Br2发生苯环取代反应生成的一溴代物的同分异构体的种数分别为
A.23.25mol 5 B.24.5mol 7
C.24.5mol 8 D.23.25mol 6
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com