
题目列表(包括答案和解析)
牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
![]()
(1)进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到损失,其原因是________.
(2)已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小,质地坚固,请用离子方程式表示,当牙膏中配有氟化物添加剂后能防止龋齿的原因________.
(3)根据以上原理,请你提供一种其他促进矿化的方法________.解析:本题考查的内容主要是电离平衡的移动和离子方程式的书写.
(1)c(OH-)减小,则平衡向脱矿方向移动.
(2)牙膏中的氟化物电离出F-,与Ca2+、PO![]() 结合成Ca5(PO4)3F更难电离.
结合成Ca5(PO4)3F更难电离.
(3)欲使平衡向矿化方向移动,应该增大c(Ca2+)或c(PO![]() ),而不宜大幅度增大c(OH-).
),而不宜大幅度增大c(OH-).
短周期元素X、Y的原子序数相差2。下列有关叙述不正确的是( )
A.X与Y可能位于同一主族
B.X与Y不一定位于同一周期
C.X与Y可能形成离子化合物XY
D.X与Y不可能形成共价化合物XY
【解析】考查元素周期表的结构,本题可采用举例排除法。H和Li的原子序数相差2,A、B正确。NaF是离子化合物,C正确。CO2是共价化合物,D错误,所以正确的答案是D。
短周期元素X、Y的原子序数相差2。下列有关叙述不正确的是( )
A.X与Y可能位于同一主族
B.X与Y不一定位于同一周期
C.X与Y可能形成离子化合物XY
D.X与Y不可能形成共价化合物XY
【解析】考查元素周期表的结构,本题可采用举例排除法。H和Li的原子序数相差2,A、B正确。NaF是离子化合物,C正确。CO2是共价化合物,D错误,所以正确的答案是D。
(8分)A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如下图所示。其中A、B、C、D在常温下都是气体,B为红棕色。
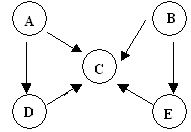
(1)写出各下列物质的化学式:则A是 D是 。
(2)写出下列反应的化学方程式:
B→C的化学方程式为 。
E→C的化学方程式为
【解析】本题属于无机框图题,做这种类型的试题,关键寻找突破点。B为红棕色,则B是NO2,这说明是N元素之间的相互转化。又因为A、B、C、D在常温下都是气体,所以A是氮气,D是氨气,C是NO,E是硝酸。二氧化氮溶于水即生成NO,稀硝酸被还原也可以生成NO。
(12分)下表是元素周期表的一部分,针对所给的11种元素,完成下列各小题。
(1)化学性质最不活泼的元素是 (填元素名称);
(2)Cl原子结构示意图为 ;
(3)第三周期元素中,最高价氧化物对应水化物碱性最强的是 (填化学式);
(4)O和N中,原子半径较大的是 ;
(5)“高钙牛奶”中的钙是指 (填“元素”或“单质”);
(6)Cl的气态氢化物的稳定性比F的气态氢化物 (填强或弱);
(7)常温下为红棕色气体的氧化物的化学式是 。
(8)镁是一种重要的金属材料,工业上采用电解熔融氯化镁获得金属镁,该反应的化学方程式为 ;
(9)S元素形成的一种氢化物的化学式是 ,该物质中H元素与S元素的质量比
m(H):m(S)= 。(相对原子质量:H-1 S-32)
【解析】考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可知最不活泼的应该是稀有气体元素Ar;Cl属于第三正确第 ⅦA,所以其原子结构示意图为;同周期元素自左向右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强。在第三周期中最活泼的金属是Na,所以氢氧化钠的碱性最强,N的原子半径大于O的原子半径;牛奶是混合物,所以“高钙牛奶”中的钙是指元素,而不是单质;同主族元素自上而下非金属性逐渐减弱,金属性逐渐增强,氯化氢的稳定性弱于氟化氢的;常温下为红棕色气体的氧化物的化学式是NO2;电解熔融氯化镁生成物是镁和氯气;S是第ⅥA,最低价是-2价,所以氢化物的化学式为H2S,其中H元素与S元素的质量比是(1×2)︰32=1︰16。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com