
题目列表(包括答案和解析)
欲测定金属镁的原子量.请利用下图给定的仪器组装一套实验装置(每件仪器只允许使用一次,假设各气体体积可看作是标准状况下测得).

填写下列各项(气体流向从左到右)
(1)各种仪器连接的先后顺序(用小写字母表示)应是________.
(2)连接好仪器后,要进行的操作有如下几步:
①待仪器B中的物质恢复至适当温度时,测得量筒C中水的体积为![]() ;
;
②擦掉镁条表面的氧化膜,将其置于天平上称量,得质量为mg,并将其投入试管B中的有孔隔板上;
③检查各装置的气密性;
④旋开仪器A上分液漏斗的活塞,使其中的水能顺利流下,当镁完全溶解时再关闭这个活塞,这时共在瓶A中放入水![]() .
.
上述操作的次序为(填序号)________.
(3)根据实验数据可算出金属镁的原子量,其数学表达式为________.
(4)若试管B的温度未冷却至室温,就测量量筒C中水的体积,这将会使所测原子量数据(填“偏高”、“偏低”、“无影响”)________;
(5)若未擦净镁条表面的氧化膜就进行实验,这将会使所测原子量数据(填“偏高”、“偏低”、“无影响”)______________.

填写下列各项(气体流向从左到右)
(1)各种仪器连接的先后顺序(用小写字母表示)应是________.
(2)连接好仪器后,要进行的操作有如下几步:
①待仪器B中的物质恢复至适当温度时,测得量筒C中水的体积为![]() ;
;
②擦掉镁条表面的氧化膜,将其置于天平上称量,得质量为mg,并将其投入试管B中的有孔隔板上;
③检查各装置的气密性;
④旋开仪器A上分液漏斗的活塞,使其中的水能顺利流下,当镁完全溶解时再关闭这个活塞,这时共在瓶A中放入水![]() .
.
上述操作的次序为(填序号)________.
(3)根据实验数据可算出金属镁的原子量,其数学表达式为________.
(4)若试管B的温度未冷却至室温,就测量量筒C中水的体积,这将会使所测原子量数据(填“偏高”、“偏低”、“无影响”)________;
(5)若未擦净镁条表面的氧化膜就进行实验,这将会使所测原子量数据(填“偏高”、“偏低”、“无影响”)______________.
实验室有一瓶Na2SO3固体,可能含有NaCl、Na2SO4、BaCl2、K2CO3、K2SO4中的一种或几种杂质,通过下列实验确定该样品的成分及Na2SO3的质量分数.
①取少量样品于试管中,加水振荡,未见沉淀生成;
②透过蓝色钴玻璃观察,焰色反应无紫色;
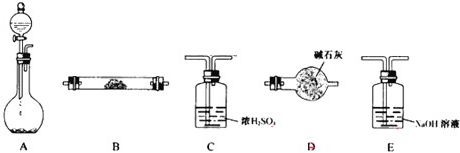
③用下图所示仪器进行合理组装,利用H2SO4(浓)+Na2SO3=Na2SO4+SO2↑+H2O,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)

请回答下列问题:
(1)按气流从左到右方向,正确的连接顺序为:A接________,________接________,________接B.
(2)利用所组装置,由分液漏斗向圆底烧瓶中滴加10 mL水,将排入量筒中________mL液体.
(3)液体X是________,其作用是________.
(4)Y的作用是防止产生的气体溶于水,下列所给试剂符合要求的是________.
A.苯 B.四氯化碳 C.酒精 D.汽油
若称取样品3.00 g,加入10.0 mol/L的硫酸5 mL(已过量),产生无色气体,排入量筒中液体的体积为229 mL(标准状况).
(5)对获得准确的气体体积无益的操作有________(填序号)
①检查装置的气密性;
②连通乙、丁的导管要预先注满水;
③读数时视线与量筒内凹液面最低点相平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出.
(6)根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是________.样品中可能有的杂质是________.
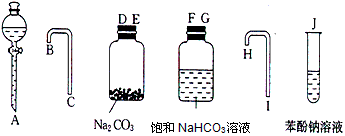

| ||
| ||
| 65Y |
| 16X |
| 65Y |
| 16X |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com