
题目列表(包括答案和解析)
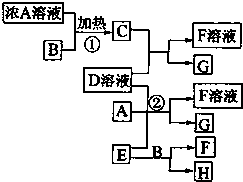 (2012?梧州模拟)有关物质存在如图所示的转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.请回答下列问题:
(2012?梧州模拟)有关物质存在如图所示的转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.请回答下列问题:

某食盐样品中混有NaBr杂质,为了测定该食盐样品的纯度,可设计实验过程如图甲所示:
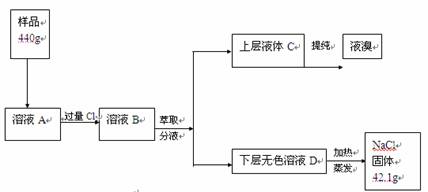
甲图
阅读上述实验过程,完成下列填空:
(1)请你从乙图中选出四个装置(可重复使用),来完成向溶液A中通入过量Cl2的实验,将所选装置的选项字母填入方框,并在括号中写出装置内所放的化学药品。
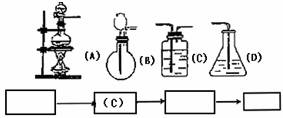
乙图
( ) (饱和食盐水)(溶液A) ( )
(2)为了证明溶液D中几乎不存在Br-,可选用的试剂为(多选不给分) __ 。(填选项字母)
A.碘水 B.淀粉碘化钾溶液
C.新制氯水和四氯化碳 D.食盐水
(3)依据甲图所示,在萃取操作中应选取的有机溶剂为(多选不给分) 。
A.四氯化碳 B.甲苯 C.乙醇 D.裂化汽油
(4)在萃取、分液的过程中,把分液漏斗玻璃塞上的凹槽对漏斗口上的小孔,其目的是 。如丙图所示,待分液漏斗内的混合液分层后,应采取的分离操作是 。
(5)加热蒸发溶液D时,除需带铁圈的铁架台、坩埚钳和火柴外,还必须用到的仪器有 、 、 。
(6)试计算原固体混合物中氯化钠的质量分数为 。
(08衡阳八中模拟)(18分)某食盐样品中混有NaBr杂质,为了测定该食盐样品的纯度,可设计实验过程如图11所示:



阅读上述实验过程,完成下列填空:
(1)请你从图12中选用四个装置(可重复使用)来完成向溶液A中通入过量Cl2的实验,将所选装置的选项字母填入方框,并在括号中写出装置内所放的化学药品。

(2) 为了证明溶液D中几乎不存在Br-,可选用的试剂为(多选不给分)______(填选项字母);
A.碘水 B.淀粉碘化钾溶液
C.新制氯水 D.食盐水
(3)依据图11所示,在萃取操作中应选取的有机溶剂为(多选不给分)_____________;
A.四氯化碳 B.甲苯
C.乙醇 D.裂化汽油
(4)在萃取、分液的过程中,把分液漏斗玻璃塞上的凹槽对准漏斗口上的小孔,其目的是: ;
如图13所示,待分液漏斗内的混合液分层后,应采取的操作是 ;
(5)加热蒸发溶液D时,除需带有铁圈的铁架台、坩埚钳和火柴外,还必须用到的仪器有 、 ____、___。
(6)试计算原固体混合物中氯化钠的质量分数为 。
下列说法正确的是 ▲ (填序号)。
①由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来
②水的沸点是100℃,酒精的沸点是78.5℃,用直接蒸馏法能使含水酒精变为无水酒精
③由于胶粒的直径比离子大,所以淀粉溶液中混有的碘化钾可用渗析法分离
④分离苯和苯酚的混合液,先加入适量浓溴水,再过滤、分液,即可实现
⑤由于高级脂肪酸钠盐在水中的分散质微粒直径在1nm~100 nm之间,所以可用食盐使高级脂肪酸纳从皂化反应后的混合物中析出
⑥不慎把苯酚溶液沾到皮肤上,应立即用酒精洗涤
⑦用稀溴水滴入苯酚溶液中制备2,4,6-三溴苯酚
⑧实验室使用体积比为1:3的浓硫酸与乙醇的混合溶液制乙烯时,为防加热时反应混合液出现暴沸现象,除了要加沸石外,还应注意缓慢加热让温度慢慢升至170℃
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com