
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
| —ı∆¯ |
| °˜ |
| ϡH2SO4 |
| ¡ÚÀ·—«Ã˙ |
| œıÀ·“¯ |
| «‚—ıªØƒ∆ |
| œ°¡ÚÀ· |
| ≈®H2SO4 |
| °˜ |
| °˜ |
| ||
| ||
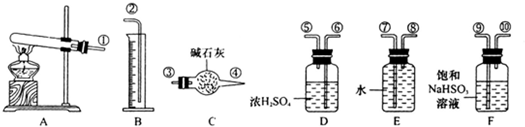
(1)œ¬¡– µ—È≤Ÿ◊˜ªÚ∂‘ µ—È ¬ µµƒ√Ë ˆ≤ª’˝»∑µƒ «________(ÃÓ–Ú∫≈,¥Ì—°“ª∏ˆµπø€2∑÷£¨≤ª≥ˆœ÷∏∫∑÷)
¢Ÿ”√¡øÕ≤¡øµ√œ°¡ÚÀ·»Ð“∫8.0mL£ª¢⁄≈®¡ÚÀ·≤ª–°–ƒ’¥‘⁄∆§∑Ù…œ£¨”¶¡¢º¥”√¥Û¡øµƒÀÆ≥Âœ¥£ª¢€”√»»µƒ≈®HClœ¥µ”∏Ω◊≈”–MnO2µƒ ‘πУª¢Ð‘⁄¡ÚÀ·Õ≠æßÃÂΩ·æßÀÆ∫¨¡øµƒ≤‚∂®÷–£¨»Ùº”»»∫ÛµƒŒÞÀÆ¡ÚÀ·Õ≠∑€ƒ©±Ì√Ê∑¢∫⁄£¨‘ÚÀ˘≤‚Ω·æßÀÆ∫¨¡øø…ƒÐª·∆´∏þ£ª¢ðFe(OH)3Ω∫ÔÎFeCl3»Ð“∫ø…”√π˝¬Àµƒ∑Ω∑®∑÷¿Î£ª¢Þ”√ºÓ ΩµŒ∂®πСøµ√KMnO4»Ð“∫20.50mL£ª¢þ µ—È “øÏÀŸ÷∆±∏…Ÿ¡øH2°¢O2°¢NH3°¢HClø…“‘”√Õ¨“ª÷÷∆¯ÃÂ∑¢…˙◊∞÷√£ª¢ý≈‰÷∆“ª∂®≈®∂»µƒ»Ð“∫ ±£¨»Ù∂®»ð ±≤ª–°–ƒº”ÀÆ≥¨π˝»ð¡ø∆øµƒøÃ∂»œþ£¨”¶¡¢º¥”√µŒπÐŒ¸»•∂ý”ýµƒ≤ø∑÷°£
(2)”–≥£”√≤£¡ß“«∆˜◊È≥…µƒœ¬¡–¡˘÷÷ µ—È◊∞÷√(∏˘æð–Ë“™ø…‘⁄∆‰÷–º”»Î“∫êÚπÃÃÂ)

¢ŸƒÐ”√◊ˆ∏…‘Ô∂˛—ıªØ¡Ú∆¯Ãµƒ◊∞÷√”–________£ª(ÃÓ¥˙∫≈£¨œ¬Õ¨)
¢⁄º»ƒÐ”√”⁄ ’ºØ¬»∆¯”÷ƒÐ”√”⁄ ’ºØ“ª—ıªØµ™∆¯Ãµƒ◊∞÷√”–________£ª
¢€‘⁄¬»∆¯∫ÕÃ˙∑¥”¶ µ—È÷–£¨ƒÐÃ̺”‘⁄÷∆∆¯∫ÕªØ∫œ∑¥”¶◊∞÷√÷ƺ‰“‘≥˝»•¬»∆¯÷–¬»ªØ«‚µ»‘”÷ ∆¯Ãµƒ◊∞÷√”–________£ª
»Ù”√C◊∞÷√◊ˆ∂˛—ıªØ¡Ú”Î…’±≠÷–«‚—ıªØƒ∆»Ð“∫∑¥”¶ µ—È£¨‘Ú∆‰÷–π„ø⁄∆øµƒ◊˜”√ «________°£
(3)—ß–£ªØ—ß–À»§–°◊È÷™µ¿∂˛—ıªØ√ÃÐ◊˜π˝—ıªØ«‚∑÷Ω‚µƒ¥þªØº¡∫Û£¨œÎ‘ŸÃΩæø∆‰À˚“ª–©ŒÔ÷ »Á—ıªØ¬¡ «∑Ò“≤ø…“‘◊˜π˝—ıªØ«‚∑÷Ω‚µƒ¥þªØº¡°£«Îƒ„“ª∆≤Œ”ÎÀ˚√«µƒÃΩæøπ˝≥ð£
¢Ÿ[Œ Â]£∫Al2O3ƒÐ≤ªƒÐ◊˜π˝—ıªØ«‚∑÷Ω‚µƒ¥þªØº¡ƒÿ£ø
¢⁄[≤¬œÎ]£∫Al2O3ƒÐ◊˜π˝—ıªØ«‚∑÷Ω‚µƒ¥þªØº¡°£
¢€[ µ—È—È÷§]£∫

¢Ð[Ω·¬€]£∫Al2O3ƒÐº”øÏπ˝—ıªØ«‚∑÷Ω‚ÀŸ¬ £¨π Al2O3ƒÐ◊˜π˝—ıªØ«‚∑÷Ω‚µƒ¥þªØº¡°£
¢ð[Ã÷¬€”Î∑¥Àº]£∫æ≠π˝Ã÷¬€£¨”–µƒÕ¨—ß»œŒ™÷ª”–…œ ˆ¡Ω∏ˆ÷§æð£¨≤ªƒÐ÷§√˜Al2O3ƒÐ◊˜π˝—ıªØ«‚µƒ¥þªØº¡£¨ªπ“™≤π≥‰“ª∏ˆÃΩæø µ—È£∫
µ—È»˝£∫[ µ—ȃøµƒ]£∫ÃΩæø________°£
[ µ—È≤Ω÷Ë]£∫¢Ÿ◊º»∑≥∆¡øAl2O3(…Ÿ¡ø)µƒ÷ ¡ø£ª¢⁄ÕÍ≥… µ—È∂˛£ª¢€¥˝∑¥”¶Ω· ¯∫Û£¨Ω´ µ—È∂˛ ‘πпԵƒŒÔ÷ Ω¯––π˝¬À°¢œ¥µ”°¢________°¢≥∆¡ø£ª¢Ð∂‘±»∑¥”¶«∞∫ÛAl2O3µƒ÷ ¡ø°£
[Ã÷¬€]£∫»Áπ˚Al2O3‘⁄∑¥”¶«∞∫Û÷ ¡ø≤ª±‰£¨‘ÚÀµ√˜Al2O3ø…“‘◊˜π˝—ıªØ«‚∑÷Ω‚µƒ¥þªØº¡°£
µ´–°ª™»œŒ™£¨“™÷§√˜≤¬œÎ£¨…œ ˆ»˝∏ˆ µ—Ȫπ≤ª◊„𪣨ªπ–Ë“™‘Ÿ‘ˆº”“ª∏ˆÃΩæø µ—È£∫ÃΩæø________°£
¡ÚªØ«‚(H2S) «“ª÷÷æþ”–≥Ùº¶µ∞∆¯Œ∂µƒŒÞ…´∆¯Ã£¨”–æÁ∂棨¥Ê‘⁄”⁄∂ý÷÷…˙≤˙π˝≥Ó‘º∞◊‘»ªΩÁ÷–°£‘⁄»Àõƒ∫Ð∂ý…˙¿Ìπ˝≥Ã÷–“≤∆◊≈÷ÿ“™◊˜”√°£
◊ ¡œ£∫¢ŸH2Sø…»Ð”⁄ÀÆ?‘º1°√2?£¨∆‰ÀƻГ∫Œ™∂˛‘™»ıÀ·°£
¢⁄H2Sø…”ΖÌ∂ýΩ Ù¿Î◊”∑¥”¶…˙≥…≥¡µÌ°£
¢€H2S‘⁄ø’∆¯÷–»º…’£¨ª—Ê≥ µ≠¿∂…´°£
(1)ƒ≥ªØ—ß–°◊ȅ˺∆¡À÷∆»°H2S≤¢—È÷§∆‰–‘÷ µƒ µ—È£¨»Áœ¬ÕºÀ˘ æ°£A÷– «CuSO4»Ð“∫£¨B÷–∑≈”– ™»Ûµƒ¿∂…´ Ø»Ô ‘÷Ω£¨C÷– «FeCl3»Ð“∫°£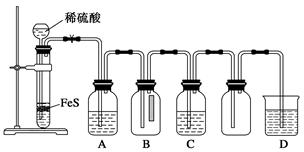
ªÿ¥œ¬¡–Œ £∫
¢ŸA÷–”–∫⁄…´≥¡µÌ(CuS)≤˙…˙£¨A÷–∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™___________________°£
¢⁄B÷–µƒœ÷œÛ «__________________°£
¢€C÷–÷ª”–«≥ª∆…´≥¡µÌ≤˙…˙£¨«“»Ð“∫±‰«≥¬Ã…´°£‘ÚC÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™______________°£
¢ÐD÷– ¢∑≈µƒ ‘º¡ø…“‘ «________(ÃÓ◊÷ƒ∏–Ú∫≈)°£
a£ÆÀÆ b£Æ—ŒÀ·
c£ÆNaCl»Ð“∫ d£ÆNaOH»Ð“∫
(2)Œ™Ω¯“ª≤ΩÃΩæø£≠2º€¡ÚµƒªØ∫œŒÔ”Σ´4º€¡ÚµƒªØ∫œŒÔ∑¥”¶Ãıº˛£¨–°√˜Õ¨—ß”÷…˺∆¡Àœ¬¡– µ—È°£
| | µ—È≤Ÿ◊˜ | µ—Èœ÷œÛ |
| µ—È1 | Ω´µ»≈®∂»µƒNa2S∫ÕNa2SO3»Ð“∫∞¥Ãª˝±»2°√1ªÏ∫œ | ŒÞ√˜œ‘œ÷œÛ |
| µ—È2 | Ω´H2SÕ®»ÎNa2SO3»Ð“∫÷– | Œ¥º˚√˜œ‘≥¡µÌ£¨‘Ÿº”»Î…Ÿ¡øœ°¡ÚÀ·£¨¡¢º¥≤˙…˙¥Û¡ø«≥ª∆…´≥¡µÌ |
| µ—È3 | Ω´SO2Õ®»ÎNa2S»Ð“∫÷– | ”–«≥ª∆…´≥¡µÌ≤˙…˙ |

¡ÚªØ«‚(H2S) «“ª÷÷æþ”–≥Ùº¶µ∞∆¯Œ∂µƒŒÞ…´∆¯Ã£¨”–æÁ∂棨¥Ê‘⁄”⁄∂ý÷÷…˙≤˙π˝≥Ó‘º∞◊‘»ªΩÁ÷–°£‘⁄»Àõƒ∫Ð∂ý…˙¿Ìπ˝≥Ã÷–“≤∆◊≈÷ÿ“™◊˜”√°£
◊ ¡œ£∫¢ŸH2Sø…»Ð”⁄ÀÆ?‘º1°√2?£¨∆‰ÀƻГ∫Œ™∂˛‘™»ıÀ·°£
¢⁄H2Sø…”ΖÌ∂ýΩ Ù¿Î◊”∑¥”¶…˙≥…≥¡µÌ°£
¢€H2S‘⁄ø’∆¯÷–»º…’£¨ª—Ê≥ µ≠¿∂…´°£
(1)ƒ≥ªØ—ß–°◊ȅ˺∆¡À÷∆»°H2S≤¢—È÷§∆‰–‘÷ µƒ µ—È£¨»Áœ¬ÕºÀ˘ æ°£A÷– «CuSO4»Ð“∫£¨B÷–∑≈”– ™»Ûµƒ¿∂…´ Ø»Ô ‘÷Ω£¨C÷– «FeCl3»Ð“∫°£
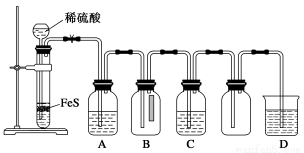
ªÿ¥œ¬¡–Œ £∫
¢ŸA÷–”–∫⁄…´≥¡µÌ(CuS)≤˙…˙£¨A÷–∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™___________________°£
¢⁄B÷–µƒœ÷œÛ «__________________°£
¢€C÷–÷ª”–«≥ª∆…´≥¡µÌ≤˙…˙£¨«“»Ð“∫±‰«≥¬Ã…´°£‘ÚC÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™______________°£
¢ÐD÷– ¢∑≈µƒ ‘º¡ø…“‘ «________(ÃÓ◊÷ƒ∏–Ú∫≈)°£
a£ÆÀÆ b£Æ—ŒÀ·
c£ÆNaCl»Ð“∫ d£ÆNaOH»Ð“∫
(2)Œ™Ω¯“ª≤ΩÃΩæø£≠2º€¡ÚµƒªØ∫œŒÔ”Σ´4º€¡ÚµƒªØ∫œŒÔ∑¥”¶Ãıº˛£¨–°√˜Õ¨—ß”÷…˺∆¡Àœ¬¡– µ—È°£
| µ—È≤Ÿ◊˜ | µ—Èœ÷œÛ |
µ—È1 | Ω´µ»≈®∂»µƒNa2S∫ÕNa2SO3»Ð“∫∞¥Ãª˝±»2°√1ªÏ∫œ | ŒÞ√˜œ‘œ÷œÛ |
µ—È2 | Ω´H2SÕ®»ÎNa2SO3»Ð“∫÷– | Œ¥º˚√˜œ‘≥¡µÌ£¨‘Ÿº”»Î…Ÿ¡øœ°¡ÚÀ·£¨¡¢º¥≤˙…˙¥Û¡ø«≥ª∆…´≥¡µÌ |
µ—È3 | Ω´SO2Õ®»ÎNa2S»Ð“∫÷– | ”–«≥ª∆…´≥¡µÌ≤˙…˙ |
“—÷™£∫µÁ¿Î∆Ω∫‚≥£ ˝£∫
H2S°°Kal£Ω1.3°¡10£≠7£¨Ka2£Ω7.1°¡10£≠15
H2SO3°°Ka1£Ω1.7°¡10£≠2£¨Ka2£Ω5.6°¡10£≠8
¢Ÿ∏˘æð…œ ˆ µ—È£¨ø…“‘µ√≥ˆΩ·¬€£∫‘⁄__________Ãıº˛œ¬£¨£´4º€¡ÚªØ∫œŒÔø…“‘—ıªØ£≠2º€¡ÚµƒªØ∫œŒÔ°£
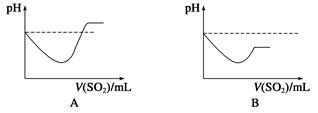
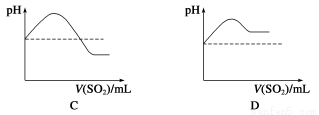
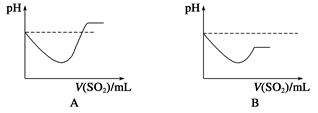
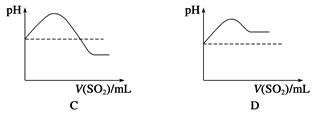
¢⁄Ω´SO2∆¯ÃÂÕ®»ÎH2SÀƻГ∫÷–÷±÷¡π˝¡ø£¨œ¬¡–±Ì æ»Ð“∫pHÀÊSO2∆¯ÃÂê˝±‰ªØπÿœµ æ“‚Õº’˝»∑µƒ «________(ÃÓ◊÷ƒ∏–Ú∫≈)°£

(3)Œƒœ◊º«‘ÿ£¨≥£Œ¬œ¬H2Sø…”ÎAg∑¢…˙÷√ªª∑¥”¶…˙≥…H2°£œ÷Ω´H2S∆¯ÃÂÕ®π˝◊∞”–“¯∑€µƒ≤£¡ßπУ¨«Î…˺∆ºÚµ• µ—È£¨Õ®π˝ºÏ—È∑¥”¶≤˙ŒÔ÷§√˜H2S”ÎAg∑¢…˙¡À÷√ªª∑¥”¶______°£
| | µ—È≤Ÿ◊˜ | µ—Èœ÷œÛ |
| µ—È1 | Ω´µ»≈®∂»µƒNa2S∫ÕNa2SO3»Ð“∫∞¥Ãª˝±»2°√1ªÏ∫œ | ŒÞ√˜œ‘œ÷œÛ |
| µ—È2 | Ω´H2SÕ®»ÎNa2SO3»Ð“∫÷– | Œ¥º˚√˜œ‘≥¡µÌ£¨‘Ÿº”»Î…Ÿ¡øœ°¡ÚÀ·£¨¡¢º¥≤˙…˙¥Û¡ø«≥ª∆…´≥¡µÌ |
| µ—È3 | Ω´SO2Õ®»ÎNa2S»Ð“∫÷– | ”–«≥ª∆…´≥¡µÌ≤˙…˙ |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com