
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
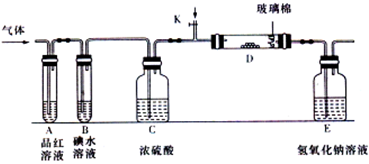
Θ®10Ζ÷Θ©”ΟΓΑΓΧΓ±ΜρΓΑΓΝΓ±≈–Εœœ¬Ν–ΥΒΖ® «Ζώ’ΐ»ΖΓΘ
Θ®1Θ©“ΜΗωD2OΖ÷Ή”ΥυΚ§ΒΡ÷–Ή” ΐΈΣ8ΓΘ
Θ®2Θ©HIΓΔHBrΓΔHClΓΔHFΒΡΈ»Ε®–‘“ά¥Έ‘ω«ΩΓΘ
Θ®3Θ©Ά§÷ςΉε‘ΣΥΊ¥”…œΒΫœ¬Θ§ΒΞ÷ ΒΡ»έΒψ÷πΫΞΫΒΒΆΓΘ
Θ®4Θ©≥ΘΈ¬œ¬Na”κΉψΝΩO2Ζ¥”Π…ζ≥…Na2OΘ§ΥφΈ¬Ε»…ΐΗΏ…ζ≥…Na2OΒΡΥΌ¬ ÷πΫΞΦ”ΩλΓΘ
Θ®5Θ©¥”ΡήΝΩΫ«Ε»Ω¥Θ§ΕœΩΣΜ·―ßΦϋ“ΣΖ≈»»Θ§–Έ≥…Μ·―ßΦϋ“ΣΈϋ»»ΓΘ“ΜΗωΜ·―ßΖ¥”Π « ΆΖ≈ΡήΝΩΘ§ΜΙ «Έϋ ’ΡήΝΩΘ§»ΓΨω”ΎΕΰ’ΏΒΡœύΕ‘¥σ–ΓΓΘ
Θ®6Θ©ΫΪ–ΩΤ§ΚΆΆ≠Τ§”ΟΒΦœΏΝ§Ϋ”Θ§≤ΔΤΫ––≤ε»κœΓΝρΥα÷–Θ§”…”Ύ–ΩΤ§ «ΗΚΦΪΘ§Υυ“‘»ή“Κ÷–ΒΡHΘΪœρΗΚΦΪ«®“ΤΓΘ
Θ®7Θ©‘ΎΕΰ―θΜ·Νρ”κ―θΤχΒΡΖ¥”Π÷–Θ§ Β±ΧαΗΏ―θΤχ≈®Ε»Θ§Ω…ΧαΗΏΕΰ―θΜ·ΝρΒΡΉΣΜ·¬ ΓΘ
Θ®8Θ©Ε଻ֹΆιΟΜ”–Ά§Ζ÷“λΙΙΧεΘ§÷ΛΟςΦΉΆιΖ÷Ή”ΨΏ”–’ΐΥΡΟφΧεΫαΙΙΓΘ
Θ®9Θ©”ΟΒψ»ΦΜρΆ®»κΥα–‘ΗΏΟΧΥαΦΊ»ή“Κ÷–ΒΡΖΫΖ®ΨυΩ…“‘Φχ±πΦΉΆιΚΆ““œ©ΓΘ
Θ®10Θ©±Ϋ≤Μ”κΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΓΔδεΥ°ΖΔ…ζΖ¥”ΠΘ§÷ΛΟς±Ϋ≤ΜΨΏ”–άύΥΤ““œ©÷–ΒΡΥΪΦϋΓΘ
ΓΨΫβΈωΓΩκ°‘≠Ή”Κ§”–1Ηω÷–Ή”Θ§Υυ“‘“ΜΗωD2OΖ÷Ή”÷–Κ§”–10Ηω÷–Ή”ΓΘΖ«Ϋπ τ–‘ «FΘΨClΘΨBrΘΨIΘ§Υυ“‘œύ”Π«βΜ·ΈοΒΡΈ»Ε®–‘÷πΫΞΦθ»θΓΘΆ§÷ςΉε‘ΣΥΊ¥”…œΒΫœ¬Θ§ΒΞ÷ ΒΡ»έΒψΩ…“‘÷πΫΞΫΒΒΆΘ§άΐ»γΒΎIAΘ§“≤Ω…“‘÷πΫΞ…ΐΗΏΘ§άΐ»γΒΎ ΔςAΓΘ‘ΎΦ”»» «ΡΤΚΆ―θΤχΒΡ…ζ≥…Έο «Ιΐ―θΜ·ΡΤΓΘΕœΩΣΜ·―ßΦϋ“ΣΈϋ»»Θ§–Έ≥…Μ·―ßΦϋ“ΣΖ≈»»ΓΘ‘Ύ‘≠Βγ≥Ί÷–Θ§ΒγΉ”¥”ΗΚΦΪΨ≠ΒΦœΏ¥ΪΒίΒΫ’ΐΦΪ…œΘ§»ή“Κ÷–ΒΡ―τάκΉ”œρ’ΐΦΪ“ΤΕ·ΓΘ‘ω¥σΖ¥”ΠΈο≈®Ε»Θ§Ω…“‘Φ”ΩλΖ¥”ΠΥΌ¬ ΓΘ»τΦΉΆι «ΤΫΟφ–ΆΫαΙΙΘ§‘ρΕ଻ֹΆι±Ί»Μ¥φ‘Ύ2÷÷Ά§Ζ÷“λΙΙΧεΓΘ““œ©Ρή ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΘ§ΦΉΆι≤ΜΩ…“‘ΓΘΆ§ ±““œ©÷–Κ§ΧΦΝΩΗΏΘ§»Φ…’ΜαΟΑ≥ωΚΎ―ΧΓΘ”…”Ύ±Ϋ÷–≤Μ¥φ‘ΎΧΦΧΦΥΪΦϋΘ§Υυ“‘≤ΜΡή ΙδεΥ°Ά …ΪΘ§“≤≤ΜΡή ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΓΘ
Θ®10Ζ÷Θ©”ΟΓΑΓΧΓ±ΜρΓΑΓΝΓ±≈–Εœœ¬Ν–ΥΒΖ® «Ζώ’ΐ»ΖΓΘ
Θ®1Θ©“ΜΗωD2OΖ÷Ή”ΥυΚ§ΒΡ÷–Ή” ΐΈΣ8ΓΘ
Θ®2Θ©HIΓΔHBrΓΔHClΓΔHFΒΡΈ»Ε®–‘“ά¥Έ‘ω«ΩΓΘ
Θ®3Θ©Ά§÷ςΉε‘ΣΥΊ¥”…œΒΫœ¬Θ§ΒΞ÷ ΒΡ»έΒψ÷πΫΞΫΒΒΆΓΘ
Θ®4Θ©≥ΘΈ¬œ¬Na”κΉψΝΩO2Ζ¥”Π…ζ≥…Na2OΘ§ΥφΈ¬Ε»…ΐΗΏ…ζ≥…Na2OΒΡΥΌ¬ ÷πΫΞΦ”ΩλΓΘ
Θ®5Θ©¥”ΡήΝΩΫ«Ε»Ω¥Θ§ΕœΩΣΜ·―ßΦϋ“ΣΖ≈»»Θ§–Έ≥…Μ·―ßΦϋ“ΣΈϋ»»ΓΘ“ΜΗωΜ·―ßΖ¥”Π « ΆΖ≈ΡήΝΩΘ§ΜΙ «Έϋ ’ΡήΝΩΘ§»ΓΨω”ΎΕΰ’ΏΒΡœύΕ‘¥σ–ΓΓΘ
Θ®6Θ©ΫΪ–ΩΤ§ΚΆΆ≠Τ§”ΟΒΦœΏΝ§Ϋ”Θ§≤ΔΤΫ––≤ε»κœΓΝρΥα÷–Θ§”…”Ύ–ΩΤ§ «ΗΚΦΪΘ§Υυ“‘»ή“Κ÷–ΒΡHΘΪœρΗΚΦΪ«®“ΤΓΘ
Θ®7Θ©‘ΎΕΰ―θΜ·Νρ”κ―θΤχΒΡΖ¥”Π÷–Θ§ Β±ΧαΗΏ―θΤχ≈®Ε»Θ§Ω…ΧαΗΏΕΰ―θΜ·ΝρΒΡΉΣΜ·¬ ΓΘ
Θ®8Θ©Ε଻ֹΆιΟΜ”–Ά§Ζ÷“λΙΙΧεΘ§÷ΛΟςΦΉΆιΖ÷Ή”ΨΏ”–’ΐΥΡΟφΧεΫαΙΙΓΘ
Θ®9Θ©”ΟΒψ»ΦΜρΆ®»κΥα–‘ΗΏΟΧΥαΦΊ»ή“Κ÷–ΒΡΖΫΖ®ΨυΩ…“‘Φχ±πΦΉΆιΚΆ““œ©ΓΘ
Θ®10Θ©±Ϋ≤Μ”κΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΓΔδεΥ°ΖΔ…ζΖ¥”ΠΘ§÷ΛΟς±Ϋ≤ΜΨΏ”–άύΥΤ““œ©÷–ΒΡΥΪΦϋΓΘ
ΓΨΫβΈωΓΩκ°‘≠Ή”Κ§”–1Ηω÷–Ή”Θ§Υυ“‘“ΜΗωD2OΖ÷Ή”÷–Κ§”–10Ηω÷–Ή”ΓΘΖ«Ϋπ τ–‘ «FΘΨClΘΨBrΘΨIΘ§Υυ“‘œύ”Π«βΜ·ΈοΒΡΈ»Ε®–‘÷πΫΞΦθ»θΓΘΆ§÷ςΉε‘ΣΥΊ¥”…œΒΫœ¬Θ§ΒΞ÷ ΒΡ»έΒψΩ…“‘÷πΫΞΫΒΒΆΘ§άΐ»γΒΎIAΘ§“≤Ω…“‘÷πΫΞ…ΐΗΏΘ§άΐ»γΒΎ ΔςAΓΘ‘ΎΦ”»» «ΡΤΚΆ―θΤχΒΡ…ζ≥…Έο «Ιΐ―θΜ·ΡΤΓΘΕœΩΣΜ·―ßΦϋ“ΣΈϋ»»Θ§–Έ≥…Μ·―ßΦϋ“ΣΖ≈»»ΓΘ‘Ύ‘≠Βγ≥Ί÷–Θ§ΒγΉ”¥”ΗΚΦΪΨ≠ΒΦœΏ¥ΪΒίΒΫ’ΐΦΪ…œΘ§»ή“Κ÷–ΒΡ―τάκΉ”œρ’ΐΦΪ“ΤΕ·ΓΘ‘ω¥σΖ¥”ΠΈο≈®Ε»Θ§Ω…“‘Φ”ΩλΖ¥”ΠΥΌ¬ ΓΘ»τΦΉΆι «ΤΫΟφ–ΆΫαΙΙΘ§‘ρΕ଻ֹΆι±Ί»Μ¥φ‘Ύ2÷÷Ά§Ζ÷“λΙΙΧεΓΘ““œ©Ρή ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΘ§ΦΉΆι≤ΜΩ…“‘ΓΘΆ§ ±““œ©÷–Κ§ΧΦΝΩΗΏΘ§»Φ…’ΜαΟΑ≥ωΚΎ―ΧΓΘ”…”Ύ±Ϋ÷–≤Μ¥φ‘ΎΧΦΧΦΥΪΦϋΘ§Υυ“‘≤ΜΡή ΙδεΥ°Ά …ΪΘ§“≤≤ΜΡή ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com