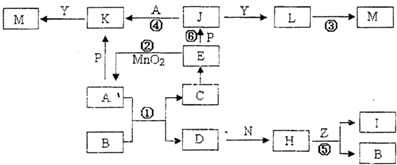
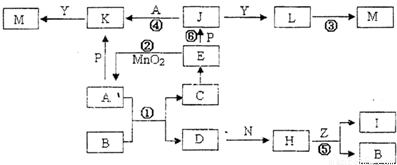
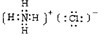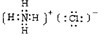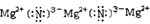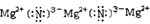常见的非金属黄色晶体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱.E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成.E被足量氢氧化钠溶液吸收得到无色溶液F.溶液F在空气中长期放置与氧气发生反应,溶液呈强碱性,生成物之一为H.H的组成元素与F相同,其结构和化学性质与过氧化钠相似,溶液显黄色.请回答下列问题:
(1)B与氢氧化钠溶液反应的化学方程式为:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
.
(2)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.该反应的氧化产物为
硫酸钠(Na2SO4)
硫酸钠(Na2SO4)
,当生成2mol二氧化氯时,转移电子
2
2
mol.
(3)溶液F在空气中长期放置生成H的化学反应方程式为:
4Na2S+O2+2H2O=4NaOH+2Na2S2(或2Na2S+O2+2H2O=4NaOH+2S,Na2S+S=Na2S2)
4Na2S+O2+2H2O=4NaOH+2Na2S2(或2Na2S+O2+2H2O=4NaOH+2S,Na2S+S=Na2S2)
.
(4)H的溶液与稀硫酸反应产生的现象为
溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
.