
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
“―÷ΣAΓΔBΓΔCΓΔDΓΔE «Ζ÷≤Φ”Ύ‘ΣΥΊ÷ήΤΎ±μ÷–»ΐΗωΕΧ÷ήΤΎΒΡ÷ςΉε‘ΣΥΊΘ§ΥϋΟ«ΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΓΘEΒΡάκΉ”‘ΎΆ§÷ήΤΎ‘ΣΥΊΒΡΦρΒΞάκΉ”÷–ΑκΨΕΉν–ΓΘ§BΓΔCΓΔD÷°Φδ“Σ–Έ≥…BDΚΆCDΦΑBD2ΚΆCD2Ζ÷Ή”ΓΘ
Θ®1Θ©–¥≥ωB‘≠Ή”ΒΡΒγΉ” ΫΘΚ Θ§CΒΞ÷ ΒΡΫαΙΙ ΫΘΚ ΓΘ
Θ®2Θ©œ¬Ν–Μ·ΚœΈοΒΡΜ·―ß Ϋ’ΐ»ΖΒΡ”–ΘΚ ΘΜ
AΘ°A2BD3 BΘ°A2B2D4 CΘ°A4BD DΘ°A2BD EΘ°A2BD4
Θ®3Θ©AΓΔDΝΫ‘ΣΥΊΡή–Έ≥…A2DΚΆA2D2ΝΫ÷÷Μ·ΚœΈοΘ§Τδ÷–A2D2Ω…Ω¥Ής»θΥαΘ§–¥≥ωΤδœύ”ΠΒΡΒγάκΖΫ≥Χ ΫΘΚ ΘΜΘ®”ΟΜ·―ßΖϊΚ≈±μ ΨΘ©
Θ®4Θ©‘ΣΥΊC”κΝΉ‘ΣΥΊœύ±»Θ§Ζ«Ϋπ τ–‘Ϋœ«ΩΒΡ « Θ®Χν‘ΣΥΊΖϊΚ≈Θ©ΓΘ
œ¬Ν–±μ ω÷–Ρή÷ΛΟς’β“Μ ¬ ΒΒΡ «ΘΚ ΓΘ
AΘ°Ά®≥ΘΧθΦΰœ¬Θ§‘ΣΥΊCΒΞ÷ ΈΣΤχΧ§Θ§ΝΉ‘ΣΥΊΒΞ÷ ΈΣΙΧΧ§
BΘ°‘ΣΥΊC–Έ≥…ΉνΗΏΦέ―θΜ·ΈοΥ°Μ·ΈοΈΣ«ΩΥαΘ§ΕχH3PO4ΈΣ÷–«ΩΥα
CΘ°‘ΣΥΊC–Έ≥…«βΜ·Έο±»ΝΉΜ·«βΈ»Ε®
DΘ°‘ΣΥΊC–Έ≥…«βΜ·ΈοΒΡΥ°»ή“Κœ‘Φν–‘
Θ®5Θ©ΧΫ―ΑΈο÷ ΒΡ–‘÷ ≤ν“λ–‘―ßœΑΒΡ÷Ί“ΣΖΫΖ®÷°“ΜΓΘBΓΔCΓΔDΓΔEΥΡ÷÷‘ΣΥΊΒΡΒΞ÷ ÷–Μ·―ßΓΔ–‘÷ Οςœ‘≤ΜΆ§ΤδΥϋ»ΐ÷÷ΒΞ÷ ΒΡ «ΘΚ Θ§άμ”…ΘΚ ΓΘ
“―÷ΣAΓΔBΓΔCΓΔD «ΕΧ÷ήΤΎ÷–ΒΡΥΡ÷÷Ζ«Ϋπ τ‘ΣΥΊΘ§ΥϋΟ«ΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§ΥΡ÷÷‘ΣΥΊΒΡ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ÷°ΚΆΈΣ16Θ§A”κBΓΔCΓΔD÷°ΦδΨυΩ…–Έ≥…Κ§”–10ΗωΒγΉ”Μρ18ΗωΒγΉ”ΒΡΜ·ΚœΈοΘ§«“AΓΔDΉι≥…ΒΡΜ·ΚœΈο‘Ύ≥ΘΈ¬œ¬≥ “ΚΧ§ΓΘ
Θ®1Θ©AΓΔCΝΫ÷÷‘ΣΥΊΉι≥…ΒΡ10ΗωΒγΉ”Μ·ΚœΈοΒΡΖ÷Ή”ΒΡΩ’ΦδΙΙ–Ά «______________Θ§ τ”Ύ________Θ®ΧνΦΪ–‘ΓΔΖ«ΦΪ–‘Θ©Ζ÷Ή”ΓΘ
Θ®2Θ©BΒΞ÷ ‘ΎΗΏΈ¬œ¬Ω…¥”A”κDΉι≥…ΒΡΡ≥÷÷Μ·ΚœΈο÷–÷ΟΜΜ≥ωAΘ§Ά§ ±…ζ≥…Μ·ΚœΈοBDΘ§ΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ__________________________ΓΘ
Θ®3Θ©AΓΔCΓΔD»ΐ÷÷‘ΣΥΊ‘≠Ή”ΑκΨΕ”…–ΓΒΫ¥σΒΡΥ≥–ρ «Θ®”Ο‘ΣΥΊΖϊΚ≈±μ ΨΘ©________________________ΘΜ”…A”κCΓΔ A”κDΙΙ≥…ΒΡΝΫ÷÷Ζ÷Ή”Θ§ΫαΚœH+ΒΡΡήΝΠ______________«ΩΘ®ΧνΜ·―ß ΫΘ©Θ§”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ’β“Μ ¬ ΒΘΚ_________________________ΓΘ
Θ®4Θ©AΓΔBΓΔD»ΐ÷÷‘ΣΥΊ–Έ≥…ΒΡΨΏ”–18ΗωΒγΉ”ΒΡΜ·ΚœΈοΒΡΫαΙΙΦρ ΫΈΣ____________________________ΓΘ
Θ®5Θ©’βΥΡ÷÷‘ΣΥΊΩ…Ήι≥…‘≠Ή”Ηω ΐ±»ΈΣ5:1:1:2Θ®Α¥AΓΔBΓΔCΓΔDΥ≥–ρΘ©ΒΡΜ·ΚœΈοΘ§ΤδΟϊ≥ΤΈΣ____________ΓΘ
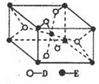
“―÷ΣAΓΔBΓΔCΓΔDΓΔEΈε÷÷‘ΣΥΊΒΡ‘≠Ή”–ρ ΐ“ά¥ΈΒί‘ω,AΓΔBΓΔCΓΔDΈΜ”ΎΕΧ÷ήΤΎΓΘA «‘≠Ή”ΑκΨΕΉν–ΓΒΡ‘ΣΥΊΘΜBΒΡΜυΧ§‘≠Ή”÷–ΒγΉ”’ΦΨί»ΐ÷÷ΡήΝΩ≤ΜΆ§ΒΡ‘≠Ή”ΙλΒάΘ§«“ΟΩ÷÷ΙλΒά÷–ΒΡΒγΉ”Ήή ΐœύΆ§ΘΜD‘≠Ή”ΒΡΚΥΆβ≥…Ε‘ΒγΉ” ΐ «Έ¥≥…Ε‘ΒγΉ” ΐΒΡ3±ΕΘΜE”–ΓΑ…ζΈοΫπ τΓ±÷°≥Τ,E4+ΚΆκ≤‘≠Ή”ΒΡΚΥΆβΒγΉ”≈≈≤ΦœύΆ§ΓΘAΓΔBΓΔD»ΐ÷÷‘ΣΥΊΉι≥…ΒΡ“Μ÷÷Μ·ΚœΈοM «–¬ΉΑ–όΨ” “÷–≥ΘΚ§”–ΒΡ“Μ÷÷”–ΚΠΤχΧεΘ§AΓΔBΝΫ÷÷‘ΣΥΊΉι≥…ΒΡ‘≠Ή”Ηω ΐ÷°±»ΈΣ1 : 1ΒΡΜ·ΚœΈοN «≥ΘΦϊΒΡ”–Μζ»ήΦΝΓΘ
«κΜΊ¥πœ¬Ν–Έ ΧβΘ®¥πΧβ ±,AΓΔBΓΔCΓΔDΓΔE”ΟΥυΕ‘”ΠΒΡ‘ΣΥΊΖϊΚ≈±μ ΨΘ©ΘΚ
(1)A2D2Ζ÷Ή”ΒΡΒγΉ” ΫΈΣ______Θ§EΒΡΜυΧ§‘≠Ή”ΒΡΆβΈßΒγΉ”≈≈≤Φ ΫΈΣ______ΓΘ
(2)BΓΔCΓΔD»ΐ÷÷‘ΣΥΊΒΡΒΎ“ΜΒγάκΡή”…–ΓΒΫ¥σΒΡΥ≥–ρΈΣ______ΓΘ
(3)ΒΞ÷ B”κCΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·ΈοΒΡ≈®»ή“ΚΈΔ»»Ζ¥”Π,ΤδΜ·―ßΖΫ≥Χ ΫΈΣ______
(4)œ¬Ν––π ω’ΐ»ΖΒΡ «______(Χν–ρΚ≈Θ©ΓΘ
aΘ° M «ΦΪ–‘Ζ÷Ή”,N «Ζ«ΦΪ–‘Ζ÷Ή” bΘ° MΚΆBD2Ζ÷Ή”÷–ΒΡ÷––Ρ‘≠Ή”Ψυ≤…”Οsp2‘”Μ·
cΘ° NΖ÷Ή”÷–Κ§”–6ΗωΠ“ΦϋΚΆ1ΗωΠ–Φϋ dΘ° BD2ΨßΧεΒΡ»έΒψΓΔΖ–ΒψΕΦ±»Εΰ―θΜ·ΙηΨßΧεΒΡΒΆ
(5) “―÷Σ:ΔΌEΒΡ“Μ÷÷―θΜ·ΈοQΘ§ΤδΨßΑϊΫαΙΙ»γΆΦΥυ Ψ

ΔΌQ(s)ΘΪ2Cl2(g)ΘΫECl4(l)ΘΪD2(g) ΓςHΘΫΘΪ140kJ/mol
ΔΎ2B(s)ΘΪD2(g)ΘΫ2BD(g) ΓςHΘΫΘ≠221kJ/mol
–¥≥ωΈο÷ QΚΆΫΙΧΩΓΔ¬»ΤχΖ¥”Π…ζ≥…“ΚΧ§ECI4ΚΆBDΤχΧεΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ__________________________
(6)‘Ύ0.5 LΒΡΟή±’»ίΤς÷–Θ§“ΜΕ®ΝΩΒΡC2ΚΆA2Ϋχ––»γœ¬Μ·―ßΖ¥”ΠΘΚC2(g) +3 A2(g)ΘΫ2CA3(g) ΓςH ΘΦ0Θ§ΤδΜ·―ßΤΫΚβ≥Θ ΐK”κΈ¬Ε»tΒΡΙΊœΒ»γœ¬±μΓΘ«κΜΊ¥πœ¬Ν–Έ ΧβΓΘ

ΔΌ ‘±»ΫœK1,K2ΒΡ¥σ–ΓΘ§K1________K2(Χν–¥ΓΑ >Γ±ΓΔΓΑ=Γ±ΜρΓΑ<Γ±Θ©ΓΘ
ΔΎ‘Ύ400Γφ ±,Β±≤βΒΟCA3ΚΆC2ΓΔA2ΒΡΈο÷ ΒΡΝΩΖ÷±πΈΣ3molΚΆ1 molΓΔ2 mol ±,‘ρΗΟΖ¥”ΠΒΡ V(C2)’ΐ_________(C2)ΡφΘ®Χν–¥ΓΑ>Γ±ΓΔΓΑ=Γ±ΜρΓΑ<Γ±Θ©ΓΘ

ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com