
题目列表(包括答案和解析)
(22分)2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol的ΔH=—99kJ·mol—1.请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol的ΔH=—99kJ·mol—1.请回答下列问题:
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(2)图中△H= KJ·mol—1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
(4)(2分)如果反应速率υ(SO2)为0.05 mol·L—1·min—1,则υ(O2)= mol·L—1·min—1、
υ(SO3)= mol·L—1·min—1;
(5)(2分)已知单质硫的燃烧热为296 KJ·mol—1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
(6)甲烷燃料电池(KOH作电解质溶液)
负极反应方程式是:
正极反应方程式是:
总反应方程式是:
(7)(2分)常温下,设pH 均为5的H2SO4和A12(SO4)3溶液中由水电离出的c(H+)分别为c1、c2,则c1:c2= 。
(8)(2分)浓度为0.5 mol/L的盐酸与等浓度的氨水溶液反应,使溶液呈中性,则混合前体积V酸________V碱(填“大于”、“小于”或“等于”)
(9)(2分)取10 mL溶液0.5 mol/L的盐酸,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=________。
(22分)2SO2(g)+O2(g) 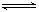 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=—99kJ·mol—1.请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=—99kJ·mol—1.请回答下列问题:
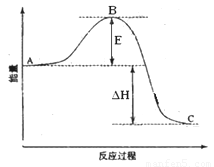
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(2)图中△H= KJ·mol—1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
(4)(2分)如果反应速率υ(SO2)为0.05 mol·L—1·min—1,则υ(O2)= mol·L—1·min—1、
υ(SO3)= mol·L—1·min—1;
(5)(2分)已知单质硫的燃烧热为296 KJ·mol—1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
(6)甲烷燃料电池 (KOH作电解质溶液)
负极反应方程式是:
正极反应方程式是:
总反应方程式是:
(7)(2分)常温下,设pH 均为5的H2SO4和A12(SO4)3溶液中由水电离出的c(H+)分别为c1 、c2,则c1:c2= 。
(8)(2分)浓度为0.5 mol/L的盐酸与等浓度的氨水溶液反应,使溶液呈中性,则混合前体积V酸________V碱(填“大于”、“小于”或“等于”)
(9)(2分)取10 mL溶液0.5 mol/L的盐酸,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=________。
(22分)2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=—99kJ·mol—1.请回答下列问题:
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(2)图中△H= KJ·mol—1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
(4)(2分)如果反应速率υ(SO2)为0.05 mol·L—1·min—1,则υ(O2)= mol·L—1·min—1、
υ(SO3)= mol·L—1·min—1;
(5)(2分)已知单质硫的燃烧热为296 KJ·mol—1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
(6)甲烷燃料电池 (KOH作电解质溶液)
负极反应方程式是:
正极反应方程式是:
总反应方程式是:
(7)(2分)常温下,设pH 均为5的H2SO4和A12(SO4)3溶液中由水电离出的c(H+)分别为c1 、c2,则c1:c2= 。
(8)(2分)浓度为0.5 mol/L的盐酸与等浓度的氨水溶液反应,使溶液呈中性,则混合前体积V酸________V碱(填“大于”、“小于”或“等于”)
(9)(2分)取10 mL溶液0.5 mol/L的盐酸,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=________。


| ||
| ||
| 实验操作 | 预期现象与结论 | ||
| 步骤1:取少量待测液放入试管1中,滴加过量lmol/L氯化钡溶液. | 若不出现浑浊,则溶液中不存在SO32-, 若出现浑浊,则溶液中可能含有SO32-. | ||
| 步骤2:若出现浑浊,静置一段时间后,将上层清液倒入试管2中.往试管1中加入蒸馏水洗涤沉淀,静置后弃去上层清液,再加入 2mol/L盐酸 2mol/L盐酸 . |
若加盐酸后出现气体,则证明溶液中存在SO32-. 若无气体,则不存在SO32-. 若加盐酸后出现气体,则证明溶液中存在SO32-. 若无气体,则不存在SO32-. | ||
| 步骤3: 在试管2中加入过量2mol/L盐酸,再滴入2滴品红,或:在试管2中加入过量lmol/L氢氧化钡溶液 在试管2中加入过量2mol/L盐酸,再滴入2滴品红,或:在试管2中加入过量lmol/L氢氧化钡溶液 |
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com