
题目列表(包括答案和解析)
电解原理在化学工业中有着广泛的应用。右图是一个电解池,a为电解液,x和y是两块电极板,通过导线与直流电源相连。回答下列问题,

(1)若X 和Y 为惰性电极,a 为饱和的氯化钠溶液,则电解池中Y电极反应式 __________________________,检验该电极反应产物的方法是_______________________________________________________。
(2)若X 和Y分别为石墨和铁,a 为饱和的氯化钠溶液,则点解过程中生成地 白色固体物质为________________________。将该物质露置在空气中,可观察到得现象为
__________________________________________________________。
(3)某同学做该实验时用铅蓄电池做电源,已知铅蓄电池的工作原理为Pb + PbO2 +2H2SO4![]() 2PbSO4+2H2O,则该蓄电池的负极反应式为_______________________________.
2PbSO4+2H2O,则该蓄电池的负极反应式为_______________________________.
若反应过程中转移的电子为0.1mol,则反应中电池内消耗的硫酸为______________.
已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4 ![]()
![]() 2PbSO4+2H2O,现以铅蓄电池作电源,用惰性电极电解100 mL 4 mol·L-1 Cu(NO3)2溶液,一定时间后在阳极收集到标准状况下气体1.12 L。
2PbSO4+2H2O,现以铅蓄电池作电源,用惰性电极电解100 mL 4 mol·L-1 Cu(NO3)2溶液,一定时间后在阳极收集到标准状况下气体1.12 L。
(1)铅蓄电池中消耗的硫酸为 mol;
(2)停止电解,向电解后的溶液中加入足量的铁粉,充分作用后溶液中的Fe2+的物质的量浓度为 mol/L(设溶液的体积不变)。
(1)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜,其工作原理如图所示。
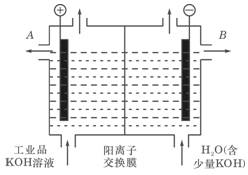
①该电解槽的阳极反应式是: 。
②除去杂质后的氢氧化钾溶液从液体出口____(填写“A”或“B”)导出。
(2)如图,有一综合电解装置,A、B、C均为0.1L 1mol/L溶液,通电一段时间后,B池溶液质量增加6.3 g,试回答:
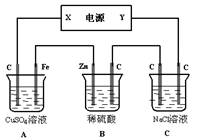
①C 池阳极放出气体在标准状况下的体积为 L ;
②A 池要恢复溶液组成,可加入 mol ;
③若电源为铅蓄电池,电极材料分别为铅和二氧化铅,以硫酸作电解质溶液,则Y极电极反应式为 ,X极质量 (填“增大”或“减小”) g。
电化学原理在工业生产中有着重要的作用,请利用所学知识回答有关问题。
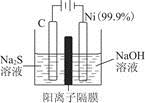
(1)用电解的方法将硫化钠溶液氧化为多硫化物的研究具有重要的实际意义,将硫化物转变为多硫化物是电解法处理硫化氢废气的一个重要内容。如是电解产生多硫化物的实验装置:
①已知阳极的反应为(x+1)S2-=Sx+S2-+2xe-,则阴极的电极反应式是____________________________
当反应转移x mol电子时,产生的气体体积为____________(标准状况下)。
②将Na2S·9H2O溶于水中配制硫化物溶液时,通常是在氮气气氛下溶解。其原因是(用离子反应方程式表示):___________________________。
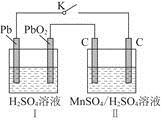
(2)MnO2是一种重要的无机功能材料,制备MnO2的方法之一是以石墨为电极,电解酸化的MnSO4溶液,阳极的电极反应式为______________________。现以铅蓄电池为电源电解酸化的MnSO4溶液,如图所示,铅蓄电池的总反应方程式为_______________________,
当蓄电池中有4 mol H+被消耗时,则电路中通过的电子的物质的量为________,MnO2的理论产量为________g。
(3)用图电解装置可制得具有净水作用的 。实验过程中,两极均有气体产生,Y极区溶液逐渐生成
。实验过程中,两极均有气体产生,Y极区溶液逐渐生成

①电解过程中,X极区溶液的pH________(填“增大”“减小”或“不变”)。
②电解过程中,Y极发生的电极反应为Fe-6e-+8OH-= +4H2O和______________________________,若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
+4H2O和______________________________,若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
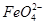 。实验过程中,两极均有气体产生,Y极区溶液逐渐生成
。实验过程中,两极均有气体产生,Y极区溶液逐渐生成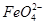
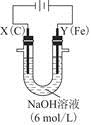
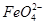 +4H2O和______________________________,若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
+4H2O和______________________________,若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com