
题目列表(包括答案和解析)
实验室常常用Cu与稀硝酸反应来制取NO气体,今有某学生设计的用氨催化氧化制取NO气体的装置示意图如下(NH3在氧化过程中转化率可达90%左右)在合成NO的反应过程中不能出现气体颜色变化,并且要观察到由合成的NO直接转化为NO2的颜色变化,已知Fe2++nNO![]() [Fe(NO)n]2+
[Fe(NO)n]2+
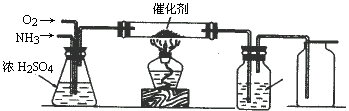
(1)你认为这套装置能达到实验目的吗?________(能,或不能)
理由是:________________
(2)如果要达到上述实验目的,如何改进,才是一套完整的实验装置?
改进方法是________________________________
改进的目的或理由是________________________________
(3)实验开始时应先________________,目的是________________

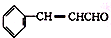 )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的: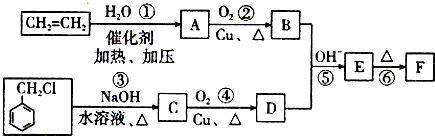
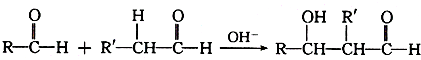
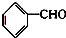

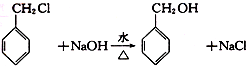

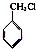 分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是
分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是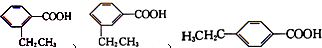 三种任写一种即可
三种任写一种即可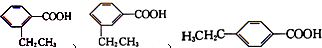 三种任写一种即可
三种任写一种即可湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com