
题目列表(包括答案和解析)
碳酸氢钠受热容易分解为碳酸钠。现加热5.00 g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.31 g,则原混合物中碳酸钠的质量为(原子量H:1 C:12 O:16 Na:23)( )
A.3.38 g B.4.58 g
C.4.16 g D.4.41 g
(原子量:H 1 C 12 O 16 Na 23)
A.3.38 g
B.4.58 g
C.4.16 g
D.4.41 g
| ||
| ||
Ⅰ.向Na2CO3溶液中滴入酚酞试液后溶液显红色,原因是(写离子方程式)_________。向上述溶液中滴入过量的CaCl2溶液,观察到的现象是__________________。
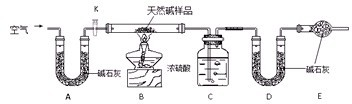
Ⅱ.某天然碱的组成为aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数)。现用下图所示装置(夹持仪器已略去)确定其组成,其中天然碱样品质量为

请回答:
(1)在用托盘天平称量样品时,如果天平指针向左偏转,说明_______________________。
(2)NaHCO3受热分解的化学反应方程式为________________________________________。
(3)E处碱石灰的作用是__________________________________________________。
(4)反应停止后打开活塞K,缓缓鼓入空气数分钟,该步骤的目的是__________________。
(5)实验结束后称得洗气瓶C质量增加
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com