
题目列表(包括答案和解析)






(1)现有A、B、C、D、E五种元素,A的原子核中没有中子;B、C元素处于同一周期,C的原子半径较小,B、C的质子数之和为27,质子数之差为5;5.4 g D的单质跟足量盐酸反应,生成D3+和6.72 L(标准状况)氢气;E和C能形成E2C型离子化合物,且E、C两元素的简单离子具有相同电子层结构.
①写出元素符号:
A________,C________,E________.
②B、D的最高价氧化物对应水化物相互反应的离子方程式为:________.
③用电子式表示C与E形成E2C的过程:________.
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.
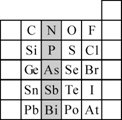
①根据元素周期律,预测:酸性强弱H3AsO4________H3PO4.(用“>”或“<”表示)
②元素S的最高正价和最低负价的代数和为________,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度________.(选填“更大”、“更小”或“相同”)
③Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是________.
 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如右(部分反应中的水已略去).
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如右(部分反应中的水已略去).

| ||
| ||
 Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体
Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体 Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体
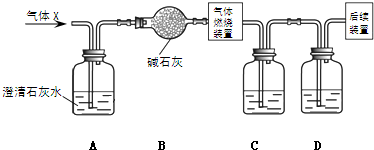
Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体 A、B、C为三种常见的单质,其中A、C为气体,B为常见金属.A溶于水所得的溶液可使石蕊试液先变红后退色.F的水溶液为浅绿色溶液,它们的关系如图:
A、B、C为三种常见的单质,其中A、C为气体,B为常见金属.A溶于水所得的溶液可使石蕊试液先变红后退色.F的水溶液为浅绿色溶液,它们的关系如图:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com