
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
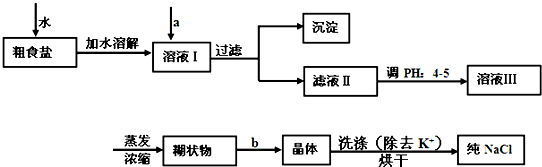
ЪГбЮЪЧШеГЃЩњЛюЕФБиашЦЗЃЌвВЪЧживЊЕФЛЏЙЄдСЯЃЎ
(1)ДжЪГбЮГЃКЌгаЩйСПCa2+ЁЂMg2+ЁЂSO42ЃЕШдгжЪРызгЃЌ
гћГ§ШЅЪГбЮжаЕФCa2+ЁЂMg2+ЁЂSO42ЃРызгЃЌЕЮМгЪдМСЫГађе§ШЗЕФЪЧ________(ЗћКЯЬѕМўЕФЖМбЁ)ЃЎ
AЃЎNa2CO3ЁЁЁЁBaCl2ЁЁЁЁNaOHЁЁЁЁHCl
BЃЎNaOHЁЁЁЁЁЁHClЁЁЁЁBaCl2ЁЁЁЁЁЁNa2CO3
CЃЎNaOHЁЁЁЁЁЁBaCl2ЁЁЁЁNa2CO3ЁЁHCl
DЃЎBaCl2ЁЁЁЁЁЁNa2CO3ЁЁNaOHЁЁЁЁHCl
(2)ЙЄвЕбЮжаКЌгаNaNO2ЃЌЭтЙлКЭЪГбЮЯрЫЦЃЌгаЯЬЮЖЃЌШЫШєЮѓЪГЛсв§Ц№жаЖОЃЌжТЫРСПЮЊ0.3 gЁЋ0.5 gЃЎвбжЊNaNO2ФмЗЂЩњШчЯТЗДгІ(ЗНГЬЪНвбХфЦН)ЃК
2NO2ЃЃЋxIЃЃЋyH+ЃН2NOЁќЃЋI2ЃЋzH2OЃЌЧыЛиД№
ИљОнЩЯЪіЗДгІЃЌПЩгУЛЏбЇЪджНКЭЩњЛюжаГЃМћЮяжЪНјааЪЕбщРДМјБ№ЙЄвЕбЮКЭЪГбЮЃЌЯжгаЕтЛЏМиЕэЗлЪджНЃЌдђЛЙашбЁгУЕФЩњЛюжаГЃМћЮяжЪЕФУћГЦЮЊ________ЃЎ
(3)гУЬсДПЕФNaClХфжЦ500 mLЁЁ4.00 molЁЄLЃ1ЁЁNaClШмвКЃЌЫљгУвЧЦїГ§вЉГзЁЂВЃСЇАєЭтЛЙга________(ЬювЧЦїУћГЦ)ЃЎ
ЕчНтБЅКЭЪГбЮЫЎЕФзАжУШчЭМЫљЪОЃЌШєЪеМЏЕФH2ЮЊ2 LЃЌдђЭЌбљЬѕМўЯТЪеМЏЕФCl2ЃМ2 LЃЌдвђЪЧ________ЃЎ

(4)ЪЕбщЪвжЦБИH2КЭCl2ЭЈГЃВЩгУЯТСаЗДгІЃК
ZnЃЋH2SO4![]() ZnSO4ЃЋH2ЁќЃЛMnO2ЃЋ4HCl(ХЈ)
ZnSO4ЃЋH2ЁќЃЛMnO2ЃЋ4HCl(ХЈ)![]() MnCl2ЃЋCl2ЁќЃЋ2H2O
MnCl2ЃЋCl2ЁќЃЋ2H2O
ОнДЫЃЌДгЯТСаЫљИјвЧЦїзАжУжабЁдёжЦБИВЂЪеМЏH2ЕФзАжУ________(ЬюДњКХ)КЭжЦБИВЂЪеМЏИЩдяЁЂДПОЛCl2ЕФзАжУ________(ЬюДњКХ)ЃЎ
ПЩбЁгУжЦБИЦјЬхЕФзАжУЃК


| ||
| ||

| ||

ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com