
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
(8Зж)AЁЂBЁЂCЁЂDЁЂEЁЂFОљЮЊЖЬжмЦкдЊЫиЃЌЦфдзгађЪ§вРДЮдіДѓЁЃвбжЊЃКAЕФзюЭтВуЕчзгЪ§ЕШгкЦфЕчзгВуЪ§ЃЛBЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФСНБЖЃЛDЪЧЕиПЧжаКЌСПзюИпЕФдЊЫиЃЛDКЭFЁЂAКЭEЗжБ№ЭЌжїзхЃЛEЪЧЫљгаЖЬжмЦкжїзхдЊЫижадзгАыОЖзюДѓЕФдЊЫиЁЃИљОнвдЩЯаХЯЂЛиД№ЯТСаЮЪЬтЃК
(1)BгыDаЮГЩЛЏКЯЮяBD2ЕФНсЙЙЪНЮЊ ЁЃ
(2)AЁЂCЁЂDШ§дЊЫиФмаЮГЩвЛжжЧПЫсМзЃЌаДГіЕЅжЪBгыМзЕФХЈШмвКЗДгІЕФЛЏбЇЗДгІЗНГЬЪН ЁЃ FB2ЦјЬхЭЈШыBaCl2КЭМзЕФЛьКЯШмвКЃЌЩњГЩАзЩЋГСЕэКЭЮоЩЋЦјЬхCDЃЌгаЙиЗДгІЕФРызгЗНГЬЪНЮЊ__________________________ЁЃ
(3)ОљгЩAЁЂDЁЂEЁЂFЫФжждЊЫизщГЩЕФСНжжбЮЃЌЦфЯрЖдЗжзгжЪСПЯрВю16ЃЌаДГіЫќУЧдкШмвКжаЯрЛЅзїгУЕФРызгЗНГЬЪНЮЊ__________________________________________ЃЛ гЩBЁЂDЁЂEзщГЩЕФбЮШмгкЫЎКѓШмвКЯдМюадЃЌЦфдвђЪЧЃЈгУРызгЗНГЬЪНБэЪОЃЉ____________________________________________________________________ЁЃ
(4)C2A4 ЉЄ ПеЦјШМСЯЕчГиЪЧвЛжжМюадШМСЯЕчГиЁЃЕчНтжЪШмвКЪЧ20ЃЅЁЋ30ЃЅЕФKOHШмвКЁЃдђШМСЯЕчГиЗХЕчЪБЃЌИКМЋЕФЕчМЋЗДгІЪНЮЊ__________________________________.ЁЃ
(8Зж)AЁЂBЁЂCЁЂDЫФжжЮяжЪжЎМфгаЯТЭМЫљЪОЕФзЊЛЏЙиЯЕЁЃвбжЊЃКAЪЧвЛжжЗЧН№ЪєЕЅжЪЃЌЮЊЛЦЩЋОЇЬхЃЛBЁЂCЁЂDОљЮЊЛЏКЯЮяЃЛBЪЧаЮГЩЫсгъЕФжївЊГЩЗжжЎвЛЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)ЛЏКЯЮяBЪЧ_______(ЬюЛЏбЇЪН,ЯТЭЌ),ЛЏКЯЮяDЪЧ___________;
(2)BЁњCЛЏбЇЗДгІЕФРраЭЪЧ________ЗДгІ(ЬюЁАЛЏКЯЁБЁЂЁАЗжНтЁБЁЂЁАжУЛЛЁБЛђЁАИДЗжНтЁБ)
(3)ЯђDЕФЯЁШмвКжаЕЮМгBaCl2ШмвКЃЌФмВњЩњАзЩЋГСЕэЁЃаДГіИУЗДгІЕФРызгЗНГЬЪНЃК
__________________________________________________ЁЃ
(8Зж)AЁЂBЁЂCЁЂDЮЊЫФжжПЩШмадЕФбЮЃЌЫќУЧЕФбєРызгЗжБ№ПЩФмЪЧBa2+ЁЂAg+ЁЂNa+ЁЂCu2+жаЕФФГвЛжжЃЌвѕРызгЗжБ№ПЩФмЪЧNO![]() ЁЂSO
ЁЂSO![]() ЁЂClЃЁЂCO
ЁЂClЃЁЂCO![]() ЕФжаЕФвЛжжЁЃ
ЕФжаЕФвЛжжЁЃ
ЂйШєАбЫФжжбЮЗжБ№ШмНтгкЪЂгаеєЦјЫЎЕФЫФжЇЪдЙмжаЃЌжЛгаCбЮЕФШмвКГЪРЖЩЋЁЃ
ЂкШєЯђЂйЕФЫФжЇЪдЙмжаЗжБ№МгШыбЮЫсЃЌBбЮЕФШмвКгаГСЕэЩњГЩЃЌDбЮЕФШмвКгаЮоЩЋЮоЮЖЕФЦјЬхвнГіЁЃ
ИљОнЂйЂкЪЕбщЪТЪЕПЩЭЦЖЯЫќУЧЕФЛЏбЇЪНЮЊЃК
ЃЈ1ЃЉA ЃЌC
ЃЈ2ЃЉаДГібЮЫсгыDЗДгІЕФРызгЗДгІЗНГЬЪНЃК
ЃЈ3ЃЉаДГіCгыBa(OH)2ШмвКЗДгІЕФРызгЗНГЬЪН
(8Зж)AЁЂBЁЂCЁЂDЫФжжЮяжЪжЎМфгаЯТЭМЫљЪОЕФзЊЛЏЙиЯЕЁЃвбжЊЃКAЪЧвЛжжЗЧН№ЪєЕЅжЪЃЌЮЊЛЦЩЋОЇЬхЃЛBЁЂCЁЂDОљЮЊЛЏКЯЮяЃЛBЪЧаЮГЩЫсгъЕФжївЊГЩЗжжЎвЛЁЃ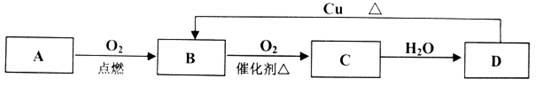
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)ЛЏКЯЮяBЪЧ_______(ЬюЛЏбЇЪН,ЯТЭЌ),ЛЏКЯЮяDЪЧ___________;
(2)BЁњCЛЏбЇЗДгІЕФРраЭЪЧ________ЗДгІ(ЬюЁАЛЏКЯЁБЁЂЁАЗжНтЁБЁЂЁАжУЛЛЁБЛђЁАИДЗжНтЁБ)
(3)ЯђDЕФЯЁШмвКжаЕЮМгBaCl2ШмвКЃЌФмВњЩњАзЩЋГСЕэЁЃаДГіИУЗДгІЕФРызгЗНГЬЪНЃК
__________________________________________________ЁЃ
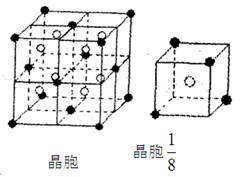
(8Зж)AЁЂBЁЂCЁЂDЁЂEЖМЪЧдЊЫижмЦкБэжаЧА20КХдЊЫиЃЌдзгађЪ§вРДЮдіДѓЃЌBЁЂCЁЂDЭЌжмЦкЃЌЃЌAЁЂDЭЌжїзхЃЌEКЭЦфЫќдЊЫиМШВЛдкЭЌжмЦквВВЛдкЭЌжїзхЃЌBЁЂCЁЂDЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяСНСНЛьКЯОљФмЗЂЩњЗДгІЩњГЩбЮКЭЫЎЁЃ
ИљОнвдЩЯаХЯЂЃЌЛиД№ЯТСаЮЪЬтЃК
(1)AКЭDЧтЛЏЮяжаЃЌЗаЕуНЯЕЭЕФЪЧ (бЁЬюЁАAЁБЛђЁАDЁБ)ЃЛAКЭBЕФРызгжаЃЌАыОЖНЯаЁЕФЪЧ (ЬюРызгЗћКХ)ЁЃ
(2)дЊЫиCдкдЊЫижмЦкБэжаЕФЮЛжУЪЧ ЁЃ
(3)AКЭEПЩзщГЩРызгЛЏКЯЮяЃЌЦфОЇАћ(ОЇАћЪЧдкОЇЬхжаОпгаДњБэадЕФзюаЁжиИДЕЅдЊ)НсЙЙШчЯТЭМЫљЪОЃЌбєРызг(гУЁАЁёЁББэЪО)ЮЛгкИУе§ЗНЬхЕФЖЅЕуЛђУцаФЃЛвѕРызг(гУЁАЉЁББэЪО)ОљЮЛгкаЁе§ЗНЬхжааФЁЃИУЛЏКЯЮяЕФЕчзгЪНЪЧ ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com