
题目列表(包括答案和解析)
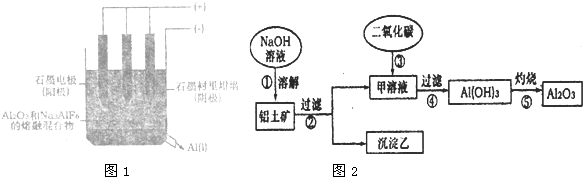
(08安师大附中二模)工业上用饱和食盐水作原料,用电解方法制取烧碱。
(1)写出电极反应和总化学方程式:阳极______________________,阴极_________________________;总反应________________________。
(2)NaOH在_________极附近生成;
(3)电极材料为石墨和铁网,阳极必须用_________,原因是
___________________________________________;
(4)电解过程中可能发生的副反应有两个,它们是:
______________________________________,
(5)若将电解槽内的隔膜去掉,同时升高电解液的温度,此时电解产物间发生反应:NaOH+Cl2→NaClO3+NaC1+H2O(未配平),假设反应进行完全,则在该条件下最后得到的两种产物的物质的量之比是______________
(6)若在NaClO3溶液中加入固体KCl,则可得到重要工业产品KClO3晶体,其原因是_______________________________________________。
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐与烧碱反应制得白色纯净的Fe(OH)2沉淀,有人设计了用电解法制备纯净的Fe(OH)2的方案,根据你所学的知识回答下列问题:(已知,两电极的材料分别为石墨和铁)
(1)电极材料的选择,阳极:_________________、阴极:____________________
电极反应式:(假若用NaOH溶液做电解质溶液)
阳极:__________________________、阴极:______________________________
(2)电解液的选择,可以是(填编号)_____________
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)做该实验时,最好在电解质溶液上覆盖一层苯,其作用为_______________________
在加苯之前, 对溶液做如何简单处理?_________________________________________
其目的是_________________________________________________________________。
(4)为了在较短时间内看到白色沉淀,可采取的措施是______________
A.改用稀硫酸做电解液 B.适当增大电源的电压
C.适当减小两电极的距离 D.适当降低电解液的浓度
| A.Ba(NO3)2 | B.BaCl2 | C.Ba(OH)2 | D.溶有NH3的BaCl2溶液 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com