
题目列表(包括答案和解析)
| 1 | 8 |
 和○代表两种不同的粒子.E与D形成的化合物的晶胞是下列中的
和○代表两种不同的粒子.E与D形成的化合物的晶胞是下列中的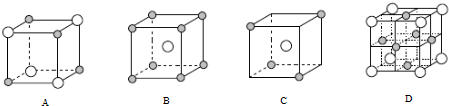
+ 4 |
+ 4 |
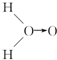 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)

(10分)配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是________。
A.CO2 B.H3O+ C.CH4 D.NH4+
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式: _____________________________。
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲: (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
乙:HOOH
化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)________________。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:_____________________________________________________________。
Ⅰ.请按下列要求写出相应粒子的电子排布式,并回答有关问题:
⑴写出基态原子或离子的电子排布式:
①Fe3+_________________; ②Cr _______________; ③Cu _______________.
⑵比较 Fe2+与Fe3+的化学稳定性:Fe2+ Fe3+,半径大小:Fe2+ Fe3+
Ⅱ⑴在第三周期中,第一电离能最小的元素是________,电负性最大的元素是________(用元素符号表示)。
⑵第二、三、周期原子中p轨道半充满的元素是_______ (用元素符号表示)。
⑶第二周期原子中,未成对电子数等于周期系数的原子有 (用元素符号表示)
Ⅲ. (2010·滁州模拟)ClO、ClO、ClO中Cl都是以sp3杂化轨道与O原子成键的,试推测下列微粒的立体结构。
| 微粒 | ClO | ClO | ClO |
| 立体结构 | | | |
(1)下列粒子中可能存在配位键的是___________。
A.CO2 B.H3O+ C.CH4 D.H2SO4
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式:_____________________________。
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初,科学家提出了两种观点:甲: 、乙:H—O—O—H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
、乙:H—O—O—H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)______________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com