
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
A.µ∞∞◊÷ »Ð“∫÷–º”»Î≈®Na2SO4»Ð“∫£¨µ∞∞◊÷ ¥”»Ð“∫÷–ƒ˝æ€∂¯Œˆ≥ˆµƒœ÷œÛΩ–—ŒŒˆ
B.…˙≥…ŒÔ÷ª”–“ª÷÷µƒªØ—ß∑¥”¶≤ª“ª∂® «ªØ∫œ∑¥”¶
C.”√…¯Œˆµƒ∑Ω∑®≥˝»•«‚—ıªØÃ˙Ω∫ÃÂ÷–µƒCl-
D.”–µÁΩ‚÷ ≤Œº”µƒªØ—ß∑¥”¶“ª∂®ø…“‘”√¿Î◊”∑Ω≥Ã Ω±Ì æ
£®13∑÷£©œ¬¡– «≤ø∑÷∂Ã÷Ð∆⁄÷–µ⁄∂˛°¢µ⁄»˝÷Ð∆⁄‘™Àÿµƒ‘≠◊”∞Îæ∂º∞÷˜“™ªØ∫œº€°£
| ‘™Àÿ¥˙∫≈ | ¢Ÿ | ¢⁄ | ¢€ | ¢Ð | ¢ð | ¢Þ | ¢þ | ¢ý |
| ‘≠◊”∞Îæ∂£®nm£© | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| ÷˜“™ªØ∫œº€ | £´1 | £´2 | £´1 | £´3 | £´5°¢ £≠3 | £´7°¢ £≠1 | £´5°¢ £≠3 | £≠2 |
| A£Æ¢€°¢¢Ð¥¶”⁄≤ªÕ¨÷Ð∆⁄ |
| B£Æ¢Þ‘⁄Õ¨÷˜◊‘™Àÿ÷–∑«Ω Ù–‘◊Ó«ø |
| C£Æ¢ð‘™Àÿ”΢þ‘™Àÿ¡Ω’þ∫ÀµÁ∫… ˝÷Æ≤Ó «8 |
| D£Æ¢Ÿ”΢ý–Œ≥…µƒªØ∫œŒÔ÷ª∫¨”–¿Î◊”º¸ |
œ¬¡–”–πÿŒÔ÷ Ω·ππ∫Õ–‘÷ µƒ– ˆ’˝»∑µƒ «£∫
¢Ÿæþ”–16∏ˆ÷ ◊”°¢16∏ˆ÷–◊”∫Õ18∏ˆµÁ◊”µƒŒ¢¡£∑˚∫≈ø…±Ì 挙£∫32 16S2-£ª
¢⁄Ù«ª˘µÁ◊” ΩŒ™£∫ £ª
£ª
¢€HClOµƒΩ·ππ Ω£∫H°™Cl°™O£ª
¢ÐNaHCO3‘⁄ÀÆ÷–µƒµÁ¿Î∑Ω≥Ã Ω£∫NaHCO3°˙Na£´£´H£´£´CO32-£ª
¢ðNa2OµƒÀƻГ∫ƒÐµºµÁ£¨’‚≤ªƒÐÀµ√˜Na2O «µÁΩ‚÷ £ª
¢ÞSiO2º»ƒÐ”Ϋ‚∑˙À·∑¥”¶”÷ƒÐ”ÎNaOH»Ð“∫∑¥”¶£¨π SiO2 «¡Ω–‘—ıªØŒÔ£ª
¢þ∑÷¡Û°¢∏…¡Û°¢¡—ªØ∂º «ªØ—ß±‰ªØ
A£Æ¢Ÿ¢⁄¢ð B£Æ¢Ÿ¢Ð¢Þ¢þ C£Æ¢⁄¢€¢Ð¢Þ D£Æ¢⁄¢€¢ð¢Þ¢þ
œ¬¡–”–πÿŒÔ÷ Ω·ππ∫Õ–‘÷ µƒ– ˆ’˝»∑µƒ «£∫
¢Ÿæþ”–16∏ˆ÷ ◊”°¢16∏ˆ÷–◊”∫Õ18∏ˆµÁ◊”µƒŒ¢¡£∑˚∫≈ø…±Ì 挙£∫32 16S2-£ª
¢⁄Ù«ª˘µÁ◊” ΩŒ™£∫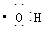 £ª
£ª
¢€HClOµƒΩ·ππ Ω£∫H°™Cl°™O£ª
¢ÐNaHCO3‘⁄ÀÆ÷–µƒµÁ¿Î∑Ω≥Ã Ω£∫NaHCO3°˙Na£´£´H£´£´CO32-£ª
¢ðNa2OµƒÀƻГ∫ƒÐµºµÁ£¨’‚≤ªƒÐÀµ√˜Na2O «µÁΩ‚÷ £ª
¢ÞSiO2º»ƒÐ”Ϋ‚∑˙À·∑¥”¶”÷ƒÐ”ÎNaOH»Ð“∫∑¥”¶£¨π SiO2 «¡Ω–‘—ıªØŒÔ£ª
¢þ∑÷¡Û°¢∏…¡Û°¢¡—ªØ∂º «ªØ—ß±‰ªØ
| A£Æ¢Ÿ¢⁄¢ð | B£Æ¢Ÿ¢Ð¢Þ¢þ | C£Æ¢⁄¢€¢Ð¢Þ | D£Æ¢⁄¢€¢ð¢Þ¢þ |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com