
题目列表(包括答案和解析)
| A、巢湖的蓝藻现象与城乡生活污水、工农业废水等的排放有关 | B、大力发展低碳经济,提倡使用太阳能、风能的城市照明系统 | C、用加酶洗衣粉可以洗毛料衣服,水温越高效果越好 | D、用硫酸亚铁和氯气处理水,既能杀菌消毒又可去除水中的悬浮物 |

化合物F是合成治疗心血管病的重要药物——美多心安的中间体.其中一种合成路线如下:
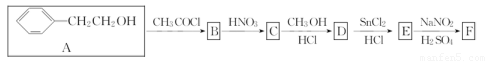
已知:
①A→B的转化中还会生成HCl。
②C的分子式为C10H11NO4,C分子的苯环上只有两种一氯代物。
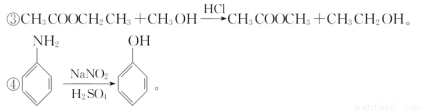
回答下列问题:
(1)A的化学名称为????????? 。
(2)C生成D的反应类型为???????? ,D生成E的反应类型为???????? 。
(3)由B生成C的化学方程式为????????????????????? 。
(4)F的结构简式为??????????? 。1mol F与足量金属钠反应产生的气体在标准状况下的体积为?????? 。
(5)B的同分异构体G既能发生银镜反应.又能发生水解反应.G的核磁共振氢谱陶中有4组吸收峰.且峰面积之比为1:2:6:3.且G分子的苯环上有3个相邻的甲基。G与足量NaOH溶液反应的化学方程式为??????????? 。
美日三名化学家[理查德·赫克(Richard Heck,美)、根岸荣—(Ei – ich Negishi,日)、铃木章(Akira Suzuki,日)利用钯(Pd)作催化剂,将有机化合物进行“裁剪”、“缝合”,创造出具有特殊功能的新物质而荣获2010年诺贝尔化学奖。赫克反应(Heck反应)的通式可表示为(R – X中的R通常是不饱和烃基或苯环;R′CH=CH通常是丙烯酸酯或丙烯腈等):

现有A、B、C、D等有机化合物有如下转化关系:
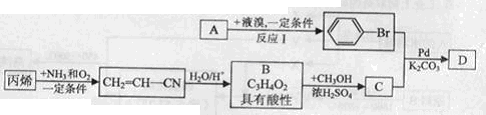
请回答下列问题:
(1)反应I的化学方程式为 。
(2)已知腈基(—C≡N)也具有不饱和性(可催化加氢),写出CH2=CH—CN完全催化加氢的化学方程式: 。
(3)丙烯腈(CH2=CH—CN)可发生加聚反应生成一种高聚物,此高聚物的结构简式为
。
(4)写出B转化为C的化学方程式: 。
(5)D的结构简式为(必须表示出分子的空间构型) 。
(6)D具有化学性质有(填编号) 。
A.加热能与氢氧化钠溶液反应
B.能使溴的四氯化碳溶液褪色
C.能发生缩聚反应和加聚反应
D.能使酸性高锰酸钾溶液褪色
(7)已知:醛基直接与苯环连接的醛如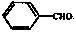 不能被新制的氢氧化铜氧化。写出同时符合下列条件的D的同分异构体的结构简式:
。
不能被新制的氢氧化铜氧化。写出同时符合下列条件的D的同分异构体的结构简式:
。
①波谱分析显示分子中没有甲基;
②1,3,5—三取代苯;
③具有酸性,既能与Fe3+作用显色,又能使溴水褪色,易被新制的氢氧化铜氧化
尿素[CO(NH2)2]是一种非常重要的高氮化肥,以天然气(含H2S)为原料 合成尿素的主要步骤如下图所示(图中某些转化步骤未列出)。

请回答下列问题:
(1)反应①的离子方程式是______________
(2)天然气脱硫后产生的Fe2S3和H2O与02反应的化学方程式是_______。
(3)反应②是放热反应,温度升高,该反应的平衡常数_______ (填 “增大”、“减小” 或“不变”)。H2NCOONH4 (氨基甲酸铵)是合成尿素的中间体,其中碳原子的杂化轨道类型是_______杂化。
(4)如果整个生产过程釆用绿色化学工艺,则生产 120t尿素理论上需要 CH4___m3 (标准状况)。
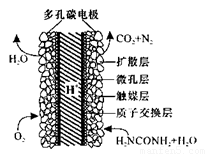
(5)化学家正在研究尿素动力燃料电池,尿液也能发电!用这种电池直接去除城市废水中的尿素,既能产生净化的水又能发电。尿素燃料电池结构如图所示,工作时负极的电极反应式为__________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com