
题目列表(包括答案和解析)
(08长沙雅礼中学一模)(16分)某课外实验小组学生利用下图所示装置进行“乙二酸(俗名草酸)晶体受热分解”的实验,并验证分解产物中有CO2和CO。(图中夹持装置已略去)
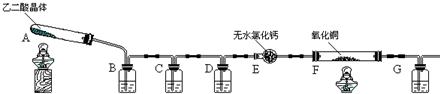 |
(1)装置C中盛放 溶液;D的作用是 ;
(2)证明分解产物中有CO的现象是 ;
(3)该装置有一个不足之处,请写出 ;
(4)某同学查阅相关资料:草酸是二元酸,酸性比碳酸强,在受热分解过程中有少量升华;草酸钙和草酸氢钙均为白色不溶物。因此该同学认为:需要在装置B之前增加一个装有________(填写下列编号字母)的洗气装置。
a.水 b.NaOH 溶液 c.Na2CO3 溶液 d.饱和NaHCO3 溶液
(5)草酸可以在酸性条件下被KMnO4氧化,反应的离子方程式为:
2MnO4- + 5H2C2O4 +6 H+ = 2Mn2+ +10 CO2↑+8 H2O
实验室常用草酸钠标定KMnO4溶液。操作如下:准确称取2.680 g草酸钠,放入锥形瓶中,加100 mL稀硫酸溶解,将锥形瓶置于 (填“酸式” “碱式”)滴定管下,用KMnO4溶液滴定。当 时,即达到滴定终点。重复上述滴定操作三次,实验数据如下表所示。
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | 第四次终点 |
滴定管 液面刻度 | 0.00 mL | 20.02 mL | 21.00mL | 19.98 mL | 20.00mL |
KMnO4溶液的物质的量浓度的是c(KMnO4)= mol?L-1。
(08长沙雅礼中学一模)(16分)短周期中的A、B、C、D、E 5种元素,原子序数逐渐增大,A、D同主族;A、B的原子序数之和等于C的原子序数;C2-离子与D+离子的核外电子数相等;B原子与D+离子核外电子数之和等于E原子的核外电子数,且D、E两元素能形成微粒个数比为1∶1的离子化合物.
(1)C的元素名称为_______。
(2)A、B元素形成化合物B2A4,其电子式为 。B2A4一空气燃料电池是一种碱性燃料电池,电解质溶液是20%一30%的KOH 溶液,放电时生成B2和水,则该燃料电池放电时,负极的电极反应式是_____。
(3)常温下用石墨为电极电解含0.2mol DE的水溶液时,阳极的电极反应式为__________,阳极产生0.2mol气体时,测得此时溶液的体积为200mL,则该溶液的pH最接近的数值为 。
(4)A、B、C、D、E中的任意三种元素可组成多种化合物,X和Y是其中的两种,X和Y都是既含离子键又含共价键的离子化合物;将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的pH<7,Y水溶液的pH>7.将0.2mol?L-1的X溶液与0.1mol?L-1的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为__________,Y的化学式为_________ 。
②混合溶液中各种带电粒子的物质的量浓度由大到小的顺序为_____________。
(08长沙雅礼中学二模)(16分)农民使用的氮肥主要是“氢铵”和尿素。某化学兴趣小组对某“氢铵”化肥进行了专项研究:
(1)预测:根据已有知识和“氢铵”的名称,该小组预测该“氢铵”是碳酸或亚硫酸或硫酸的铵盐。
(2)验证和探究:
①NH4+的验证:取少量固体药品于试管中,然后 __________。
②阴离子的探究:
 a.取少量固体药品于试管中,然后向试管中滴加稀盐酸,固体全部溶解,将产生的气体通入下列装置。观察到的现象是:溴水无明显变化,澄清石灰水变浑浊。再向滴加稀盐酸反应后的试管中,加Ba(OH)2溶液,无明显现象。
a.取少量固体药品于试管中,然后向试管中滴加稀盐酸,固体全部溶解,将产生的气体通入下列装置。观察到的现象是:溴水无明显变化,澄清石灰水变浑浊。再向滴加稀盐酸反应后的试管中,加Ba(OH)2溶液,无明显现象。
初步结论:“氢铵”是 的铵盐。
b.要进一步确定“氢铵”的成分还需要补做如下实验:取适量“氢铵”配制成溶液,取试液于一支洁净的试管中,加 (写出加入试剂后看到的现象和结论)
(3)该实验小组设计了以下二个实验方案测定该化肥的含氮量,请你阅读后解释方案中提出的问题并进行评价:

方案(一)
准确称取一定质量的样品,放入上图方案(一)的烧瓶中,滴加过量NaOH浓溶液,充分微热,按如图装置,通过实验测定烧杯增加的质量(忽略漏斗中附着溶液的质量)。然后进行计算,可得化肥的含氮量。
方案(二)准确称取一定质量的样品,放入上图方案(二)的烧瓶中,滴加过量NaOH浓溶液,充分微热,按如图装置(A管可以上下移动),测量生成的氨气体积(设所测体积为标准状况下的体积)。然后进行计算,可得化肥的含氮量。
方案(二)
图中导管a的作用是 。
请你评价上述两套方案是否合理。若合理只需要说明结论;若不合理,请简要说明原因,并指出修改方案(若要添加仪器、药品,请说明添加的位置、名称)
方案(一) 。
方案(二) 。
(08长沙雅礼中学一模)(12分)有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
阳离子 | K+ Ba2+ Cu2+ Al3+ |
阴离子 | SO42- HCO3- NO3- OH- |
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液逐滴滴入到C溶液中出现白色沉淀,继续滴加至过量,沉淀质量继续增加但沉淀的总物质的量却减少;
③进行焰色反应,A、B、C为紫色(透过蓝色钴玻璃);
④各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根椐上述实验填空:
⑴写出B、D的化学式:B ,D 。
⑵将含1 mol A的溶液与含1 mol E的溶液混合其离子方程式为 。
⑶将E溶液逐滴滴入到含一定量C的溶液中沉淀质量达到最大值时的离子方程式为 。
(08长沙雅礼中学一模)将一定体积的某NaOH溶液分成两等份,一份用PH=2的一元酸HA溶液中和,消耗酸溶液的体积为V1;另一份用PH=2的一元酸HB溶液中和,消耗酸溶液体积为V2,则下列叙述正确的是( )
A、若V1>V2,则说明HA的酸性比HB的酸性弱
B、若V1>V2,则等物质的量浓度的NaA溶液碱性比NaB溶液碱性弱
C、不论两种酸是强是弱,因为溶液PH相等,中和碱时所耗体积V1=V2
D、若将两种溶液等体积混合,混合液的PH一定等于2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com