
题目列表(包括答案和解析)
下列离子方程式正确的是
| A.鸡蛋壳浸泡在盐酸中产生气泡:CO32—+2H+===CO2↑+H2O |
| B.小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O |
| C.碘化亚铁溶液中通入少量Cl2:Cl2+2I-===2Cl-+I2 |
| D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4? + 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O |
下列离子方程式正确的是
A.鸡蛋壳浸泡在盐酸中产生气泡:CO32—+2H+===CO2↑+H2O
B.小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O
C、碘化亚铁溶液中通入少量Cl2:Cl2+2I-===2Cl-+I2
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4− + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
| A.鸡蛋壳浸泡在盐酸中产生气泡:CO32—+2H+===CO2↑+H2O |
| B.小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O |
| C.碘化亚铁溶液中通入少量Cl2:Cl2+2I-===2Cl-+I2 |
| D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4? + 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O |
根据下表提供的材料,下列叙述中,正确的是 ( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | FeCl2 | ||
| ② | KMnO4 | H2O2 | H2SO4 | O2 | MnSO4 |
| ③ | KClO3 | HCl(浓) | Cl2 | Cl2 | |
| ④ | KMnO4 | HCl(浓) | Cl2 | MnCl2 |
A.表中第①组反应的氧化产物只有FeCl3(实为Fe3+)
B.氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+
C.表中第③组反应的氧化产物与还原产物的质量之比为6:1
D.④的离子方程式配平后,H+的化学计量数应为16
某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验。
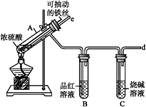
图1 图2
(1)比较两实验装置,图2装置的优点是:
①能更好地吸收有毒气体SO2,防止其污染环境;
② 。
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻止SO2气体逸出而污染环境;二是 。
(3)能说明有SO2气体产生的实验现象是 。
(4)反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+。
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
| A.稀HCl溶液 | B.稀H2SO4溶液 | C.KSCN溶液 | D.KMnO4溶液 |
 Fe(SCN)3。
Fe(SCN)3。 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com