
题目列表(包括答案和解析)
㈠2SO2(g)+O2(g) ![]() 2SO3(g)反应过程的能量变化如图
2SO3(g)反应过程的能量变化如图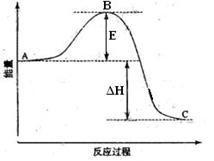 所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.
所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.
请回答下列问题:
⑴图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
⑵图中△H= KJ·mol-1;
⑶已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求写出计算过程)。
 ㈡进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,表中是部分化学键的键能数据:
㈡进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,表中是部分化学键的键能数据:
| 化学键 | P—P | P—O | O==O | P==O |
| 键能/kJ·mol-1 | 197 | 360 | 499 | x |
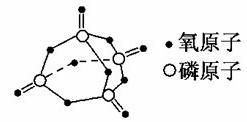
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图Ⅲ所示,则上表中x=________。
将化学知识系统化,有助于对化学问题的进一步认识和理解.
资料1:化学反应的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应.能引发化学反应的碰撞称之为有效碰撞.
资料2:化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.
资料3:化学反应的能量变化(ΔH)与反应物和生成物的键能有关.在热力学标准态(298 K、1.01×105 Pa)下,由稳定的单质发生反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH).
根据以上资料回答下列问题:
(1)下图是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(选填“A”、“B”或“C”);

(2)下图是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________;

(3)下表是部分化学键的键能数据:
![]()
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构(P4O10)如图所示,则上表中X=________.

(4)下图为氧族元素的氢化物a、b、c、d的生成热数据示意图.请你归纳:非金属元素的氢化物的稳定性与氢化物的生成热(ΔH)之间的关系:________.

将化学知识系统化,有助于对化学问题的进一步认识和理解.
资料1:化学反应的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应.能引发化学反应的碰撞称之为有效碰撞.
资料2:化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.
资料3:化学反应的能量变化(ΔH)与反应物和生成物的键能有关.在热力学标准态(298 K、1.01×105 Pa)下,由稳定的单质发生反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH).
根据以上资料回答下列问题:
(1)下图是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(选填“A”、“B”或“C”);

(2)下图是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________;

(3)下表是部分化学键的键能数据:
![]()
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构(P4O10)如图所示,则上表中X=________.

(4)下图为氧族元素的氢化物a、b、c、d的生成热数据示意图.请你归纳:非金属元素的氢化物的稳定性与氢化物的生成热(ΔH)之间的关系:________.

| |||||||||||||||||||
将化学知识系统化,有助于对化学问题的进一步认识和理解。
资料1:化学反应的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞。
资料2:化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。
资料3:化学反应的能量变化(ΔH)与反应物和生成物的键能有关。在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物的反应热叫该化合物的生成热(ΔH)。
根据以上资料回答下列问题:
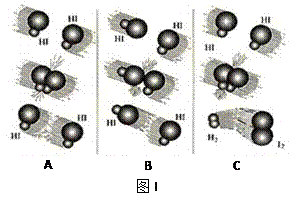
(1)图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是
__________________(选填“A”、“B”或“C”);
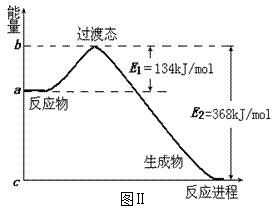
(2)图Ⅱ是1molNO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO
反应的热化学方程式:
___________________________________________;
(3) 下表是部分化学键的键能数据:

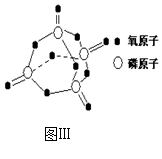
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构(P4O10)如图Ⅲ所示,则上表中
X=_______________________________。
(4)图Ⅳ为氧族元素的氢化物a、b、c、d的生成热数据示意图。
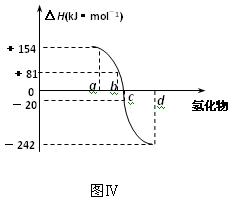
请你归纳:非金属元素的氢化物的稳定性与氢化物的生成热(ΔH)
之间的关系:_____________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com