
题目列表(包括答案和解析)
(10分)黄血盐[亚铁氰化钾,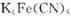 ]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为
]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为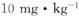 。黄血盐易溶于水,在水溶液中会电离出
。黄血盐易溶于水,在水溶液中会电离出 和
和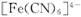 ,其中
,其中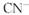 的电子式为
的电子式为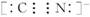 。它与硫酸反应的化学方程式为
。它与硫酸反应的化学方程式为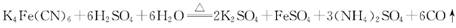
(1) 上述反应是否为氧化还原反应?______ (填“是”或“不是”)。
(2) 食盐经长时间火炒,“亚铁氰化钾”名称前的“亚铁”就去掉了,变成了剧毒物质氰化钾,这是因为黄血盐在超过400 "C1时会分解,试配平该反应的化学方程式:
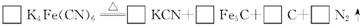
(3) 黄血盐可与高锰酸钾溶液反应,其化学方程式为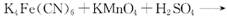
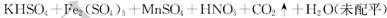
①该反应的氧化产物有______(填化学式)。
②若有1mol K4Fe(CN)6被高锰酸钾氧化,则消耗高锰酸钾的物质的量为______mol。
( 10分)低碳经济呼唤新能源和清洁环保能源。煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题。已知:CO(g) + H2O(g) H2(g) + CO2(g) △H= a kJ·mol-1 的平衡常数随温度的变化如下表:
H2(g) + CO2(g) △H= a kJ·mol-1 的平衡常数随温度的变化如下表:
|
温度/℃ |
400 |
500 |
850 |
|
平衡常数 |
9.94 |
9 |
1 |
(1)上述正反应方向是 反应(填“放热”或“吸热”)。
t1℃时物质浓度(mol/L)的变化

|
时间(min) |
CO |
H2O |
CO2 |
H2 |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
|
5 |
0.116 |
0.216 |
0.084 |
|
|
6 |
0.096 |
0.266 |
0.104 |
|
(2) t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。①与2min时相比,3min时密闭容器中混合气体的平均摩尔质量 (填增大、减小或不变)。
②表中3 min~4 min之间反应处于 状态;CO的体积分数 16% (填大于、小于或等于)。
③反应在4 min~5 min,平衡向逆方向移动,可能的原因是____(单选),表中5 min~6 min之间数值发生变化,可能的原因是______(单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
(3)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为 。
(10分)某有机物A,在不同条件下反应分别生成B1和C1,B2和C2;而B1和C1在一定条件下又能分别转化为B2和C2,C2能进一步氧化,反应如下:
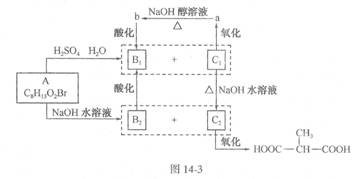 又知:Bl能使溴水褪色,又可与碳酸钠溶液反应放出CO2。试回答:
又知:Bl能使溴水褪色,又可与碳酸钠溶液反应放出CO2。试回答:
(1)B2属于 ,
C1属于
(填写序号)
A.溴代饱和一元醇
B. 溴代不饱和一元醇
C.饱和一元醇
D.不饱和一元醇
E.溴代饱和羧酸盐 F. 溴代不饱和羧酸盐 G. 饱和羧酸盐 H.不饱和羧酸盐
(2)写出A、B1、C2的结构简式:
A B1 C2 。
(3)写出下列反应的化学方程式:
①a→b .
②C1→C2
。
(10分)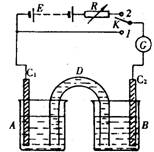 装置如右图:D是允许通过离子的盐桥,E是48V稳压电源,R是可变电阻,K是开关,G是灵敏电流计,C1、C2是碳棒,A、B是烧杯。
装置如右图:D是允许通过离子的盐桥,E是48V稳压电源,R是可变电阻,K是开关,G是灵敏电流计,C1、C2是碳棒,A、B是烧杯。
1.已知AsO43-+2I-+2H+![]() AsO33-+I2+H2O是可逆反应。若A中盛KI-I2溶液,B中盛Na3AsO4和Na3AO3溶液,则当K接1,并向B中滴加浓盐酸时发现G中的指针发生偏转;改向B中滴加40%的NaOH溶液时,G中的指针则向反方向偏转。
AsO33-+I2+H2O是可逆反应。若A中盛KI-I2溶液,B中盛Na3AsO4和Na3AO3溶液,则当K接1,并向B中滴加浓盐酸时发现G中的指针发生偏转;改向B中滴加40%的NaOH溶液时,G中的指针则向反方向偏转。
(1)两次操作过程中指针偏转的原因是
(2)指针偏转方向相反的原因是
(3)加盐酸时C1上发生的反应是
(4)加NaOH溶液时C1上发生的反应是
2.当 A中盛适量的1mol/L Na2SO4溶液,B中盛40mL适量浓度的KI-KHCO3溶液,且K接2时,可用该装置来测定砷的含量。其操作如下:称取5.00g含砷样品,溶解后加入还原剂,使砷全部转化为HAsO32-,除去过量的还原剂后再转移到250mL容量瓶中配成250mL溶液,用移液管从中取出10mL加入B中,边搅拌边电解,电解生成的 I2可将HAsO32-快速、定量地氧化为HAsO42-,以2mA的电流电解241s便可使反应进行完全。
(1)反应到达终点时宜用 来指示;
(2)假设电能没有损失,试求样品中As2O5的质量分数。
(10分)黄血盐[亚铁氰化钾,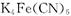 ]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为
]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为
 。黄血盐易溶于水,在水溶液中会电离出
。黄血盐易溶于水,在水溶液中会电离出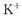 和
和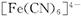 ,其中
,其中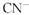 的电子式为
的电子式为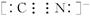 。它与硫酸反应的化学方程式为
。它与硫酸反应的化学方程式为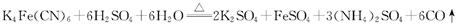
(1) 上述反应是否为氧化还原反应?______ (填“是”或“不是”)。
(2) 食盐经长时间火炒,“亚铁氰化钾”名称前的“亚 铁”就去掉了,变成了剧毒物质氰化钾,这是因为黄血盐在超过400 "C1时会分解,试配平该反应的化学方程式:
铁”就去掉了,变成了剧毒物质氰化钾,这是因为黄血盐在超过400 "C1时会分解,试配平该反应的化学方程式: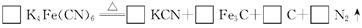
(3) 黄血盐可与高锰酸钾溶液反应,其化学方程式为
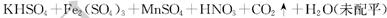
①该反应的氧化产物有______(填化学式)。
②若有1mol K4Fe(CN)6被高锰酸钾氧化,则消耗高锰酸钾的物质的量为______mol 。
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com