
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
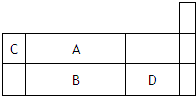 ”“±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì∂Ã÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿA°¢B°¢C°¢DÀƒ÷÷‘™Àÿµƒ– ˆ’˝»∑µƒ «£®°°°°£©
”“±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì∂Ã÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿA°¢B°¢C°¢DÀƒ÷÷‘™Àÿµƒ– ˆ’˝»∑µƒ «£®°°°°£©| A | D | |||
| E | G | M |
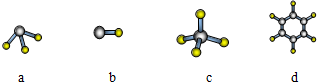
 ”“±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì«∞Àƒ÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿR°¢W°¢X°¢Y°¢ZŒÂ÷÷‘™Àÿµƒ– ˆ÷–£¨’˝»∑µƒ «£®°°°°£©
”“±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì«∞Àƒ÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿR°¢W°¢X°¢Y°¢ZŒÂ÷÷‘™Àÿµƒ– ˆ÷–£¨’˝»∑µƒ «£®°°°°£© ”“±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì«∞Àƒ÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿR°¢W°¢X°¢Y°¢ZŒÂ÷÷‘™Àÿµƒ– ˆ÷–£¨’˝»∑µƒ «£®°°°°£©
”“±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì«∞Àƒ÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿR°¢W°¢X°¢Y°¢ZŒÂ÷÷‘™Àÿµƒ– ˆ÷–£¨’˝»∑µƒ «£®°°°°£© 26°¢”“±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì«∞Àƒ÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿR°¢W°¢X°¢Y°¢ZŒÂ÷÷‘™Àÿµƒ– ˆ÷–£¨’˝»∑µƒ «£®°°°°£©
26°¢”“±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì«∞Àƒ÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿR°¢W°¢X°¢Y°¢ZŒÂ÷÷‘™Àÿµƒ– ˆ÷–£¨’˝»∑µƒ «£®°°°°£©π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com