
题目列表(包括答案和解析)
磷在氧气中燃烧,可能生成两种固态氧化物。3.1 g的单质磷(P)在3.2 g 的氧气中燃烧,至反应物耗尽,并放出X kJ热量。
(1)通过计算确定反应产物的组成(用化学式表示)是______________,其相应的质量为________。
(2)已知单质磷的燃烧热为Y kJ·mol-1,则1 mol P与O2反应生成固态P2O3的反应热ΔH=________。
(3)写出1 mol P与O2反应生成固态P2O3的热化学方程式:________________。
命题意图:本题以磷为载体,考查燃烧热、盖斯定律及热化学方程式的有关知识,重点是考查燃烧热定义和盖斯定律的理解和应用,而涉及磷的知识并不复杂。
 (2010?烟台一模)硫酸工厂周围的空气中有较多的二氧化硫.某研究性学习小组为了测定空气
(2010?烟台一模)硫酸工厂周围的空气中有较多的二氧化硫.某研究性学习小组为了测定空气 某同学欲用Cu与浓H2SO4反应制备SO2,并通过一定装置除去制得的SO2中存在的少量水蒸气和O2,以此来探究SO2能使品红褪色的具体情况以及能否对发黄的小麦秸秆进行漂白,设计装置如图所示,请完成下列问题.
某同学欲用Cu与浓H2SO4反应制备SO2,并通过一定装置除去制得的SO2中存在的少量水蒸气和O2,以此来探究SO2能使品红褪色的具体情况以及能否对发黄的小麦秸秆进行漂白,设计装置如图所示,请完成下列问题.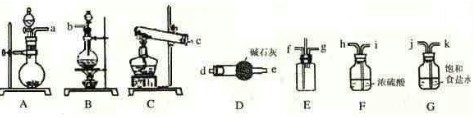
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com