
题目列表(包括答案和解析)
某校化学研究性学习小组要利用已经学过的化学知识制取少量漂白粉,并进一步探究漂白粉的化学性质。他们查阅资料得知:
![]() 该反应属于放热反应,温度稍高时便发生副反应:
该反应属于放热反应,温度稍高时便发生副反应:![]() 。学生设计出了甲、乙、丙三套装置:
。学生设计出了甲、乙、丙三套装置:

(1)请从甲、乙、丙各套装置中选取合理的部分,按气体从左至右的流向组装成一套较合理的装置(填各部分仪器的字母编号) 。
(2)部分学生认为上述组装仍存在缺点,他们指出在前两个仪器之间应增加如下装置:
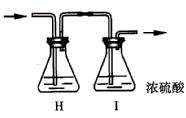
你认为H洗气瓶中所盛液体是 ,其作用是 ,若无此装置,对制漂白粉有什么不利影响 。洗气瓶I有无必要 ,理由是 。
(3)为了研究所制得的漂白粉的化学性质,同学们把少量漂白粉投入到淡绿色的![]() 溶液中,所产生的现象是 。由此可知漂白粉溶液所具有的化学性质是 。
溶液中,所产生的现象是 。由此可知漂白粉溶液所具有的化学性质是 。
某校化学研究性学习小组要利用已经学过的化学知识制取少量漂白粉,并进一步探究漂白粉的化学性质。他们查阅资料得知:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O是放热反应,温度稍高时便发生副反应:6Cl2+6Ca(OH)2→Ca(ClO3)2+5CaCl2+6H2O。学生设计出了甲、乙、丙三套装置:
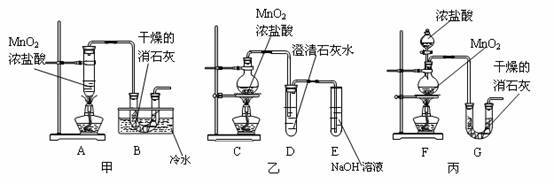
(1)请从甲、乙、丙各套装置中选取合理的部分,按气体从左至右的流向组装成一套较合理的装置,(填各部分仪器的编号)
(2)部分学生认为上述组装仍存在缺点,他们指出在前两个仪器之间应增加如下装置:
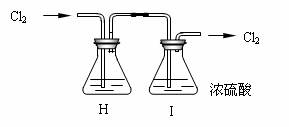
你认为H洗气瓶中所盛液体是 ,其作用是 。
若无此装置,对制漂白粉有什么不利影响 ;
洗气瓶I有无必要 理由是 。
(3)为了研究所制得的漂白粉的化学性质,同学们把少量漂白粉投入到淡绿色的FeCl2溶液,所产生的现象是 。由此可知漂白粉溶液所具有化学性质是 。


某校研究性学习小组设计了如图所示装置进行有关实验,实验时将分液漏斗中A逐滴加入烧瓶B中,(图中铁架台、铁夹已略去,要求填写的试剂的均填化学式)

(1)若A为浓硫酸,B为第三周期金属元素的单质,
其在常温下难与水反应;C为品红溶液,实验
观察到C中溶液褪色,则B是 ,简述判断B的理由 ,
若使C试管溶液恢复原来的颜色,可采取的操作为 。
(2)若B为块状大理石,C为饱和Na2CO3溶液,实验中观察到小试管内溶液变浑浊,则C试管中发生反应的化学方程式为 。
(3)若B是生石灰,实验中观察到C溶液中先形成沉淀,而后沉淀溶解,当溶液恰好澄清时,关闭E,然后将C放入盛有沸水的烧杯中,静止片刻,观察到试管壁上出现光亮银镜。则A是 ,C是 与葡萄糖的混合液。仪器D在此实验中的作用是 。
(4)利用此套装置设计实验证明碳酸、醋酸、苯酚的酸性强弱,则A、B、C中放的试剂分别是 、 、 ,B、C的实验现象分别为B 、C 。若使现象明显,放入C中的溶液应是稀溶液还是浓溶液 。(填浓或稀)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com