
题目列表(包括答案和解析)
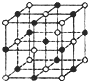 (2012?聊城一模)氯、氧、碳、铁是与人类生产生活息息相关的化学元素.
(2012?聊城一模)氯、氧、碳、铁是与人类生产生活息息相关的化学元素.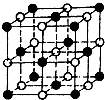 (2012?枣庄二模)碳、氧、氯、铁是与人类生产、生活息息相关的化学元素.
(2012?枣庄二模)碳、氧、氯、铁是与人类生产、生活息息相关的化学元素.如图,直线交点处的圆圈为NaCl晶体中Na+和Cl-所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。
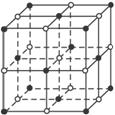
(1)请将其中代表Na+的圆圈涂黑(不考虑体积大小),以完成NaCl晶体结构示意图。
(2)晶体中,在每个Na+周围与它最接近的且距离相等的Na+共有( )
A.4个 B.6个 C.8个 D.12个
(3)晶体中,与每个Na+距离相等且距离最近的n个Cl-所围成的空间几何构型为( )
A.正四面体 B.正六面体
C.正八面体 D.正二十面体
(4)晶体中每一个重复的结构单元叫晶胞。在NaCl晶胞中正六面体的顶点上、面上、棱上的Na+或Cl-为该晶胞与其相邻的晶胞所共有,一个晶胞中Cl-的个数等于________个,即________(填计算式),Na+的个数等于___________,即________________________________(填计算式)。
(5)设NaCl的摩尔质量为M g·mol-1,食盐晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA。食盐晶体中两个距离最近的Na+中心的距离为___________cm。
 (2013?辽宁一模)[化学--选修3物质结构与性质]
(2013?辽宁一模)[化学--选修3物质结构与性质]| 417×1030 |
| a3NA |
| 417×1030 |
| a3NA |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com