
题目列表(包括答案和解析)
| ||
| ||
| 0.36-(12.8-w)/32 |
| V×1×10 -3 |
| 0.36-(12.8-w)/32 |
| V×1×10 -3 |
(8分)蛋壳的主要成分是CaCO3,其次是MgCO3、蛋白质、色素等。为测定其中钙的含量,洗净蛋壳,加水煮沸约5 min,置于蒸发皿中用小火烤干,研细。
(1) 称取0.3 g(设为0.3000g)蛋壳样品,置于锥形瓶中逐滴加入已知浓度c(HCl)的盐酸40.00 mL,而后用小火加热使之溶解,冷却后加2滴甲基橙溶液,用已知浓度c(NaOH)回滴,消耗V(NaOH) L达终点。
① (2分)写出计算钙含量的算式。
② (1分)计算得到的是钙的含量吗?
③ (1分)是原蛋壳中钙的含量吗?
(2) 称取0.3 g(设为0.3000 g)蛋壳样品,用适量强酸溶解,然后加(NH4)2C2O4得沉淀,经过滤、洗涤,沉淀溶于H2SO4溶液,再用已知浓度c(KMnO4)滴定(生成Mn2+和CO2),消耗V(KMnO4)L达到终点。
① (2分)写出计算钙含量的算式;
② (2分)此法求得的钙含量略低于上法。为什么?
(8分)、奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是:食品与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。实验操作步骤:
(1)样品处理:准确称取一定量的固体样品奶粉,移入干燥的凯氏烧瓶中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
(2)NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸铵,再经过碱化蒸馏后,氨即成为游离状态,游离氨经硼酸吸收。
(3)氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,从消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水?
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
A、凯氏烧瓶中溶液转移移到容量瓶中时,未洗涤凯氏烧瓶
B、定容时,俯视刻度线 C、定容时,仰视刻度线 D、移液时,有少量液体溅出
 (3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。(已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3)
(3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。(已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3)
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。其实凯氏定氮法的缺陷并不难弥补,只要先用三氯乙酸处理样品。三氯乙酸能让蛋白质形成沉淀,过滤后,分别测定沉淀和滤液中的氮含量,就可以知道蛋白质的真正含量和冒充蛋白质的氮含量。试求三聚氰胺中氮的含量为 。
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康
(1)含有较多______________的水称为硬水,硬水加热后产生沉淀的离子方程式为__________________________( 写出生成一种沉淀物的即可) 。
(2)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:
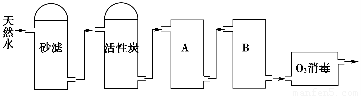
①活性炭的作用是__________________;O3消毒的优点是________________。
②A、B中放置的物质名称分别是:A__________________;B_______________。A、B中放置的物质是否可以互换?请说明原因________________________________________。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留, 从而获得纯净水的方法称为?????????????????? 。电渗析法净化水时, 使离子通过半透膜的推动力是??????????????????? ? 。
(4)检验蒸馏水的纯度时, 最简单易行的方法是测定水的 ?????????????? 。
(5)某 城 市 用 水 中c(Ca2+)为1.0×10-3mol/L, c(Mg2+)为5.0×10-4mol/L,c(HCO3_)为8.0×10-4mol/L。如用药剂软化该1000L ,应加入Ca(OH) 2???????????? g , Na2CO 3 __________ g 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com