
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
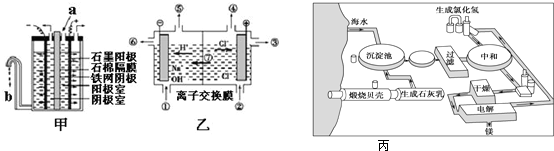
ЃЈЙВ10ЗжЃЉдквЛЖЈЬѕМўЯТЃЌНЋ3molA КЭ1mol B СНжжЦјЬхЛьКЯгкЙЬЖЈШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌЗЂЩњШчЯТЗДгІЃК3AЃЈgЃЉ+BЃЈgЃЉ
 xCЃЈgЃЉ+ 2DЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌЩњГЩ0.8mol D ЃЌВЂВтЕУCЕФХЈЖШЮЊ0.2molЁЄLЃ1ЁЃЧыЬюПеЃК
xCЃЈgЃЉ+ 2DЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌЩњГЩ0.8mol D ЃЌВЂВтЕУCЕФХЈЖШЮЊ0.2molЁЄLЃ1ЁЃЧыЬюПеЃК
ЃЈ1ЃЉx=__________
ЃЈ2ЃЉЮТЖШНЕЕЭЃЌЦНКтЯђгввЦЖЏЃЌдђе§ЗДгІЪЧ_____ЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉЗДгІЁЃ
ЃЈ3ЃЉBЕФзЊЛЏТЪЮЊ_________ЁЃ
ЃЈ4ЃЉФмХаЖЯИУЗДгІДяЕНЦНКтзДЬЌЕФвРОнЪЧ________ЃЈЬюБрКХЃЉ
A. ЛьКЯЦјЬхЕФУмЖШВЛБф
B. ШнЦїжаЕФбЙЧПВЛдйБфЛЏ
C. ЩњГЩDЕФЗДгІЫйТЪЪЧЩњГЩBЕФЗДгІЫйТЪЕФ2БЖ
D. ЕЅЮЛЪБМфФкЩњГЩ3molAЃЌЭЌЪБЩњГЩ1molB
ЃЈ5ЃЉ2minФкЦНОљЫйТЪv(A)ЃН____________________________________ЁЃ
(10Зж)ЁЂдк537ЁцЁЂ1.01ЁС105PaЪБЃЌЭљШнЛ§ПЩБфЕФУмБеШнЦїжаГфШы1molXКЭ3molYЃЌДЫЪБШнЛ§ЮЊVLЁЃБЃГжКуЮТКубЙЃЌЗЂЩњЗДгІX(g)+ 3Y(g) 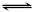 2Z(g)ЃЌДяЕНЦНКтЪБЃЌЦНКтЛьКЯЦјЬхжаZЕФЬхЛ§ЗжЪ§ЮЊ0.5ЁЃ
2Z(g)ЃЌДяЕНЦНКтЪБЃЌЦНКтЛьКЯЦјЬхжаZЕФЬхЛ§ЗжЪ§ЮЊ0.5ЁЃ
ЃЈ1ЃЉДяЕНЦНКтЪБЃЌXЕФзЊЛЏТЪдМЮЊ ЁЃ
ЃЈ2ЃЉБЃГжЩЯЪіЮТЖШКЭбЙЧПКуЖЈВЛБфЃЌШєЯђШнЦїжажЛГфШы4molZЃЌдђЗДгІДяЕНЦНКтЪБЃЌЦНКтЦјЬхжаYЕФЬхЛ§ЗжЪ§ЮЊ ЃЌШнЦїЕФШнЛ§ЮЊ LЁЃ
ЃЈ3ЃЉШєСэбЁвЛШнЛ§ЙЬЖЈВЛБфЕФУмБеШнЦїЃЌШдПижЦЮТЖШВЛБфЃЌЪЙ2molXКЭ6molYЗДгІЃЌДяЕНЦНКтЪБЦНКтЦјЬхжаZЕФЬхЛ§ЗжЪ§ШдЮЊ0.5ЃЌдђИУУмБеШнЦїЕФШнЛ§ЮЊ
ЃЈ4ЃЉШєЮТЖШШдЮЊ537ЁцЃЌШнЦїЬхЛ§БЃГжVLВЛБфЃЈКуШнЃЉЃЌЭљЦфжаГфШыa mol XЕФb mol YЃЌЪЙЗДгІДяЕНЦНКтЃЌетЪБЦНКтЦјЬхжаZЕФЬхЛ§ЗжЪ§ШдЮЊ0.5ЃЌЬхЯЕбЙЧПЮЊ1.01ЁС105PaЃЌШєa : b =" 1" : 3ЃЌдђa=
ЃЈЙВ10ЗжЃЉдквЛЖЈЬѕМўЯТЃЌНЋ3molA КЭ1mol B СНжжЦјЬхЛьКЯгкЙЬЖЈШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌЗЂЩњШчЯТЗДгІЃК3AЃЈgЃЉ+BЃЈgЃЉ xCЃЈgЃЉ+ 2DЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌЩњГЩ0.8mol D ЃЌВЂВтЕУCЕФХЈЖШЮЊ0.2molЁЄLЃ1ЁЃЧыЬюПеЃК
xCЃЈgЃЉ+ 2DЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌЩњГЩ0.8mol D ЃЌВЂВтЕУCЕФХЈЖШЮЊ0.2molЁЄLЃ1ЁЃЧыЬюПеЃК
ЃЈ1ЃЉx=__________
ЃЈ2ЃЉЮТЖШНЕЕЭЃЌЦНКтЯђгввЦЖЏЃЌдђе§ЗДгІЪЧ_____ЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉЗДгІЁЃ
ЃЈ3ЃЉBЕФзЊЛЏТЪЮЊ_________ЁЃ
ЃЈ4ЃЉФмХаЖЯИУЗДгІДяЕНЦНКтзДЬЌЕФвРОнЪЧ________ЃЈЬюБрКХЃЉ
A. ЛьКЯЦјЬхЕФУмЖШВЛБф
B. ШнЦїжаЕФбЙЧПВЛдйБфЛЏ
C. ЩњГЩDЕФЗДгІЫйТЪЪЧЩњГЩBЕФЗДгІЫйТЪЕФ2БЖ
D. ЕЅЮЛЪБМфФкЩњГЩ3molAЃЌЭЌЪБЩњГЩ1molB
ЃЈ5ЃЉ2minФкЦНОљЫйТЪv(A)ЃН____________________________________ЁЃ
(10ЗжЃЉдкГЃЮТЯТЃЌFeгыЫЎВЂВЛЦ№ЗДгІЃЌЕЋдкИпЮТЯТЃЌFeгыЫЎеєЦјПЩЗЂЩњЗДгІЁЃгІгУЯТСазАжУЃЌдкгВжЪВЃСЇЙмжаЗХШыЛЙдЬњЗлКЭЪЏУоШоЕФЛьКЯЮяЃЌМгШШЃЌВЂЭЈШыЫЎеєЦјЃЌОЭПЩвдЭъГЩИпЮТЯТЁАFeгыЫЎеєЦјЕФЗДгІЪЕбщЁБЁЃЧыЛиД№ИУЪЕбщжаЕФЮЪЬтЁЃ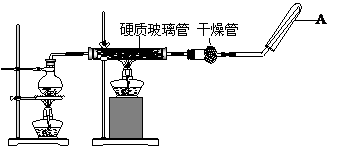
ЃЈ1ЃЉаДГіИУЗДгІЕФЗДгІЗНГЬЪН ЃЛ
ЃЈ2ЃЉдВЕзЩеЦПжаЪЂзАЕФЫЎЃЌИУзАжУЪмШШКѓЕФжївЊзїгУЪЧ ЃЛЩеЦПЕзВПЗХжУСЫМИЦЌЫщДЩЦЌЃЌЦфзїгУЪЧ ЁЃ
ЃЈ3ЃЉЪдЙмжаЪеМЏЦјЬхЪЧ ЃЌШчЙћвЊдкAДІВЃСЇЙмДІЕуШМИУЦјЬхЃЌдђБиаыЖдИУЦјЬхНјаа ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com