
题目列表(包括答案和解析)
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 0.255 | 0.385 | 0.459 |
| 生成气体/ml | 280 | 336 | 336 |
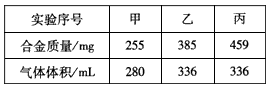
在标准状况下进行甲、乙、丙三组实验,三组各取30mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
实验序号 甲 乙 丙
合金质量(mg) 255 385 195
生成气体体积(mL) 280 336 336
(1)甲组实验中,盐酸________(填“过量”“适量”或“不足量”),理由是________。
乙组实验中,盐酸________(填“过量”“适量”或“不足量”),理由是________。要 算出盐酸的物质的量浓度,题中可作计算依据的数据是________,求得盐酸的物质的 量浓度为________。
(2)求合金中Mg、A1的物质的量之比,题中可作计算依据的数据是________,求得 的Mg、A1的物质的量之比为________。
(3)在丙组实验之后,向容器中加入1mo1·L—1的氢氧化钠溶液,能使合金中的铝恰好溶解,不形成含铝的沉淀,并使Mg2+刚好沉淀完全,再过滤出不溶固体,求滤液中各溶质的物质的量和所加入氢氧化钠溶液的体积(写计算过程)。
在标准状况下进行甲、乙、丙三组实验,三组各取30mL同浓度的盐酸溶液,加入同一种镁、铝合金粉末,产生气体,有关数据列表如下:
实验序号 甲 乙 丙
合金质量/mg 255 385 459
生成气体体积/mL 280 336 336
(1)甲组实验中,盐酸________(填“过量”或“不足”)。理由是_________________________
________________________________。
乙组实验中,盐酸_________(同上)。理由是__________________。
要算出盐酸的物质的量浓度,题中可作计算依据的数据是________,求得的盐酸的物质的量浓度为_______。
(2)求合金中Mg,Al的物质的量之比,题中可作计算依据的数据是________,求得的Mg,Al物质的量之比为________。
实验序号 甲 乙 丙
合金质量(mg) 255 385 195
生成气体体积(mL) 280 336 336
(1)甲组实验中,盐酸________(填“过量”“适量”或“不足量”),理由是________。
乙组实验中,盐酸________(填“过量”“适量”或“不足量”),理由是________。要 算出盐酸的物质的量浓度,题中可作计算依据的数据是________,求得盐酸的物质的 量浓度为________。
(2)求合金中Mg、A1的物质的量之比,题中可作计算依据的数据是________,求得 的Mg、A1的物质的量之比为________。
(3)在丙组实验之后,向容器中加入1mo1·L—1的氢氧化钠溶液,能使合金中的铝恰好溶解,不形成含铝的沉淀,并使Mg2+刚好沉淀完全,再过滤出不溶固体,求滤液中各溶质的物质的量和所加入氢氧化钠溶液的体积(写计算过程)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com