
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
| ||
| ||
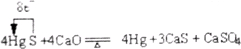
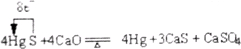
Ι· «÷Τ‘λΒγ≥ΊΓΔΒγΦΪΦΑΈ¬Ε»ΦΤΒ»ΒΡ÷Ί“Σ‘≠ΝœΘ§ΙΛ“Β…œ÷Τ¥÷Ι·ΒΡΝς≥ΧΈΣΘΚ
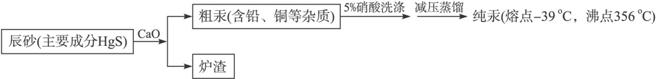
œ¬Ν–Ζ÷Έω’ΐ»ΖΒΡ «
A.≤…”Ο≥Ϋ…ΑΓΔ…ζ ·Μ“ΜλΚœ±Κ…’…ζ≥…Θ§Εχ≤Μ”Ο‘ΎΩ’Τχ÷±Ϋ”ΉΤ…’Θ§“ρΈΣ≥Ϋ…Α‘ΎΩ’Τχ÷–Φ”»»≤ΜΖ¥”Π
B.≥Ϋ…Α”κ―θΜ·ΗΤΦ”»»Θ§Ζ¥”ΠΒΡΖΫ≥Χ ΫΩ…ΡήΈΣΘΚ4HgS+4CaO====4Hg+3CaS+CaSO4
C.œ¥Β”¥÷Ι·Ω…”Ο5%ΒΡ―ΈΥα¥ζΧφ5%ΒΡœθΥα
D.‘Ύ±±ΦΪΩΦ≤λΩ… Ι”ΟΥ°“χΈ¬Ε»ΦΤ
Ι· «÷Τ‘λΒγ≥ΊΓΔΒγΦΪΦΑΈ¬Ε»ΦΤΒ»ΒΡ÷Ί“Σ‘≠ΝœΘ§ΙΛ“Β…œ÷Τ¥÷Ι·ΒΡΝς≥ΧΈΣΘΚ
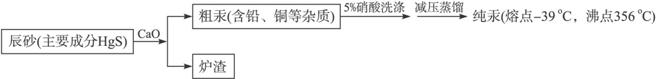
œ¬Ν–Ζ÷Έω’ΐ»ΖΒΡ «
A.≤…”Ο≥Ϋ…ΑΓΔ…ζ ·Μ“ΜλΚœ±Κ…’…ζ≥…Θ§Εχ≤Μ”Ο‘ΎΩ’Τχ÷±Ϋ”ΉΤ…’Θ§“ρΈΣ≥Ϋ…Α‘ΎΩ’Τχ÷–Φ”»»≤ΜΖ¥”Π
B.≥Ϋ…Α”κ―θΜ·ΗΤΦ”»»Θ§Ζ¥”ΠΒΡΖΫ≥Χ ΫΩ…ΡήΈΣΘΚ4HgS+4CaO====4Hg+3CaS+CaSO4
C.œ¥Β”¥÷Ι·Ω…”Ο5%ΒΡ―ΈΥα¥ζΧφ5%ΒΡœθΥα
D.‘Ύ±±ΦΪΩΦ≤λΩ… Ι”ΟΥ°“χΈ¬Ε»ΦΤ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com