
题目列表(包括答案和解析)
(6分)
(1)NaHCO3的水溶液呈 (填“酸”、“中”、“碱”)性,实验室保存NaHCO3溶液的试剂瓶应用 塞,原因
(写出有关的离子方程式,下同);Al2(SO4)3显酸性,溶液蒸干最后得到的固体产物是
;
(2) 普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是
。
(6分)(1)FeCl3水溶液呈 性,原因是(用离子方程式表示) 。
为了防止发生水解,可以加入少量的 。
(2)把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)除去MgCl2溶液中的少量FeCl3杂质可选择的合理试剂是 。
(1)配平该反应并标出电子转移的方向和数目:KMnO4+HCl = MnCl2+ KCl+ Cl2↑+ H2O
(2)氧化剂是________________,氧化产物是__________________ (填化学式)。
(3)若生成71 g Cl2消耗的HCl是___________________,被氧化的HCl是_______________。
(4)CS2(液体)能在O2中完全燃烧,生成CO2和SO2,若将0.1 mol CS2在1 mol O2中完全燃烧,所得混合气体在标准状况下所占的体积为__________L。
Ⅱ、(6分)(1)下列A. B. C. D 是中学常见的混合物分离或提纯的基本装置
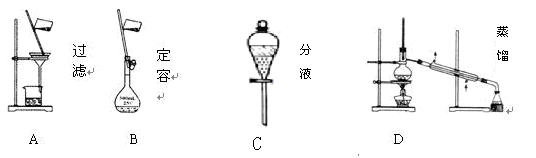
请根据实验需要将A. B.C. D装置填入适当的空格中。
①分离汽油和氯化钠溶液____________________
②用自来水制取蒸馏水__________________
③除去粗盐溶液中悬浮的泥沙_______________________________
(2)检验Fe3+常用的试剂除碱外,还可以将KSCN溶液滴入待检测溶液中,其产生的现象是______
________________________,发生反应的离子方程式________________________________。
(6分)
(1)NaHCO3的水溶液呈 (填“酸”、“中”、“碱”)性,实验室保存NaHCO3溶液的试剂瓶应用 塞,原因
(写出有关的离子方程式,下同);Al2(SO4)3显酸性,溶液蒸干最后得到的固体产物是
 ;
;
(2)普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是
。
(6分)
(1) NaHCO3的水溶液呈 (填“酸”、“中”、“碱”)性,实验室保存NaHCO3溶液的试剂瓶应用 塞,原因
(写出有关的离子方程式,下同);Al2(SO4)3显酸性,溶液蒸干最后得到的固体产物是
;
(2) 普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com