
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
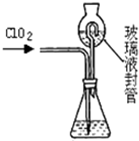 ¢Ò£Æ≤£¡ß∞Ù «ªØ—ß µ—È÷–≥£”√µƒ“«∆˜£¨∆‰◊˜”√ «”√”⁄Ω¡∞Ë°¢π˝¬ÀªÚ◊™“∆“∫౓˝¡˜£Æœ¬¡–”–πÿ µ—Èπ˝≥Ã÷–£¨øœ∂®≤ª–Ë“™ π”√≤£¡ß∞ÙΩ¯––≤Ÿ◊˜µƒ «
¢Ò£Æ≤£¡ß∞Ù «ªØ—ß µ—È÷–≥£”√µƒ“«∆˜£¨∆‰◊˜”√ «”√”⁄Ω¡∞Ë°¢π˝¬ÀªÚ◊™“∆“∫౓˝¡˜£Æœ¬¡–”–πÿ µ—Èπ˝≥Ã÷–£¨øœ∂®≤ª–Ë“™ π”√≤£¡ß∞ÙΩ¯––≤Ÿ◊˜µƒ «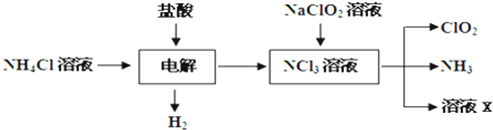
£®∞¸¿®2–°Ã‚£¨¬˙∑÷π≤10∑÷£©
¢Ò.≤£¡ß∞Ù «ªØ—ß µ—È÷–≥£”√µƒ“«∆˜£¨∆‰◊˜”√ «”√”⁄Ω¡∞Ë°¢π˝¬ÀªÚ◊™“∆“∫౓˝¡˜°£œ¬¡–”–πÿ µ—Èπ˝≥Ã÷–£¨øœ∂®≤ª–Ë“™ π”√≤£¡ß∞ÙΩ¯––≤Ÿ◊˜µƒ «_______________________£®ø…“‘∂ý—°£©
A.”√pH ‘÷Ω≤‚∂®Na2CO3»Ð“∫µƒpH
B.¥”¬»À·ºÿ∫Õ∂˛—ıªØ√Ã÷∆»°—ı∆¯µƒ £”ýπÃÃÂ÷–÷»°KCl
C. µ—È “”√–¬÷∆µƒFeSO4»Ð“∫∫Õ‘§¥¶¿Ìπ˝µƒNaOH»Ð“∫÷∆±∏Fe(OH)2∞◊…´≥¡µÌ
D.≈‰÷∆“ª∂®ŒÔ÷ µƒ¡ø≈®∂»µƒ¬»ªØƒ∆»Ð“∫
E.»°ƒ≥»Ð“∫◊ˆ—Ê…´∑¥”¶ µ—È£¨Àµ√˜∏√»Ð“∫÷–∫¨”–ƒ∆‘™Àÿ
F.”√ ¡øµƒ’·Ã«°¢≈®¡ÚÀ·∫ÕÀÆ‘⁄–°…’±≠÷–Ω¯––≈®¡ÚÀ·µƒÕ—ÀÆ–‘ µ—È
G.¥Ÿ ππ˝±•∫ÕµƒœıÀ·ºÿ»Ð“∫Œˆ≥ˆæßÃÂ
H.”√«„Œˆ∑®Ω¯––∑÷¿Î°¢œ¥µ”ø≈¡£Ωœ¥Ûµƒ≥¡µÌ
¢Ú£Æ∂˛—ıªØ¬»£®ClO2£© «“ª÷÷‘⁄ÀÆ¥¶¿Ìµ»∑Ω√Ê”–π„∑∫”¶”√µƒ∏þ–ß∞≤»´œ˚∂溡°£ClO2 «“ª÷÷ª∆¬Ã…´µƒ∆¯Ã£¨“◊»Ð”⁄ÀÆ°£ µ—È ““‘NH4Cl°¢—ŒÀ·°¢NaClO2£®—«¬»À·ƒ∆£©Œ™‘≠¡œ÷∆±∏ClO2µƒ¡˜≥ûÁœ¬£∫

¢≈–¥≥ˆµÁΩ‚ ±∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫ £ª
¢∆≥˝»•ClO2÷–µƒNH3ø…—°”√µƒ ‘º¡ « £ª£®ÃÓ–Ú∫≈£©
A£Æ±•∫Õ ≥—ŒÀÆ B£ÆºÓ ت“ C£Æ≈®¡ÚÀ· D£ÆÀÆ
¢«≤‚∂®ClO2£®»Á”“Õº£©µƒπ˝≥ûÁœ¬£∫‘⁄◊∂–Œ∆ø÷–º”»Î◊„¡øµƒµ‚ªØºÿ£¨”√100mLÀÆ»ÐΩ‚∫Û£¨‘Ÿº”3mL¡ÚÀ·»Ð“∫£ª‘⁄≤£¡ß“∫∑‚πÐ÷–º”»ÎÀÆ£ªΩ´…˙≥…µƒClO2∆¯ÃÂÕ®π˝µºπБ⁄◊∂–Œ∆ø÷–±ªŒ¸ ’£ªΩ´≤£¡ß∑‚πÐ÷–µƒÀÆ∑‚“∫µπ»Î◊∂–Œ∆ø÷–£¨º”»Îº∏µŒµÌ∑€»Ð“∫£¨”√cmol/L¡Ú¥˙¡ÚÀ·ƒ∆±Í◊º»Ð“∫µŒ∂® (I2+2S2O32£≠=2I£≠ +S4O62£≠)£¨π≤”√»•VmL¡Ú¥˙¡ÚÀ·ƒ∆»Ð“∫°£¢Ÿ◊∞÷√÷–≤£¡ß“∫∑‚πеƒ◊˜”√ « £ª
¢⁄«Î–¥≥ˆ…œ ˆ∂˛—ıªØ¬»∆¯Ã”ε‚ªØºÿ»Ð“∫∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω °° °°£ª
¢€≤‚µ√ClO2µƒ÷ ¡øm(ClO2)= °££®”√∫¨c°¢Vµƒ¥˙ ˝ Ω±Ì æ£©
œ¬¡– µ—È≤Ÿ◊˜ƒÐπª¥ÔµΩ µ—ȃøµƒµƒ «
A£Æ”√º§π‚± º¯±µÌ∑€»Ð“∫∫Õ’·Ã«»Ð“∫
B£Æ µ—È “≤…”√œ¬ÕºÀ˘ æ◊∞÷√ ’ºØSO2
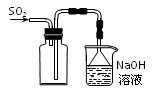
C£Æ≥˝»•NaHCO3»Ð“∫÷–µƒNa2CO3£¨ø…º”»ÎCa(OH)2»Ð“∫∫Ûπ˝¬À
D£Æ≈‰÷∆“ª∂®ŒÔ÷ µƒ¡ø≈®∂»»Ð“∫ ±£¨»ð¡ø∆ø”√’Ù¡ÛÀÆœ¥µ”∫Û‘Ÿ”√¥˝◊∞»Ð“∫»Ûœ¥
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com