
题目列表(包括答案和解析)
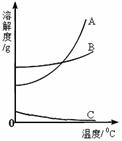
根据下面的溶解度表与溶解度曲线回答下列问题。
| 温度/℃ 溶解度 /g 物质 | 0 | 20 | 40 | 60 | 80 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.116 | 0.094 |
(1)B是________的溶解度曲线。
(2)40 ℃时,氯化钠的溶解度________(填“大于”、“小于”或“等于”)硝酸钾的溶解度。
(3)硝酸钾中混有少量的氯化钠,想要得到纯净的硝酸钾的方法是________。
(4)欲使硝酸钾的不饱和溶液转化为饱和溶液,可以采取的方法之一是________________。

(5)如右图所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入生石灰后,烧杯A中变浑浊,可能的原因是______(填字母)。
A.反应消耗水,氢氧化钙析出
B.反应放热,温度升高,氢氧化钙溶解度降低
C.生石灰与水反应生成的氢氧化钙不再溶解
根据下面的溶解度表与溶解度曲线回答下列问题:
|
| 0 | 20 | 40 | 60 | 80 | ||||||||||||||||
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | ||||||||||||||||
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | ||||||||||||||||
| Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.116 | 0.094 |

(1)B是______的溶解度曲线。
(2)40℃时,氯化钠的溶解度______(大于、小于或等于)硝酸钾的溶解度。
(3)硝酸钾中混有少量的氯化![]() 钠,想要得到纯净的硝酸钾的方法是 。
钠,想要得到纯净的硝酸钾的方法是 。
(4)欲使硝酸钾的不饱和溶液转化为饱和溶液,可以采取的方法之一是 。
(5)如右图所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入生石灰后,烧杯A中变浑浊,可能的原因是______(填序号)。
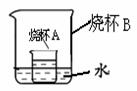 A.反应消耗水,氢氧化钙析出
A.反应消耗水,氢氧化钙析出
B.反应放热,温度升高,氢氧化钙溶解度降低
C.生石灰与水反应生成的氢氧化钙不再溶解
根据![]() 下面的溶解度表与溶解度曲线回答下列问题:
下面的溶解度表与溶解度曲线回答下列问题:
|
| 0 | 20 | 40 | 60 | 80 | ||||||||||||||
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | ||||||||||||||
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | ||||||||||||||
| Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.116 | 0.094 |
(1)B是______的溶解度曲线。
(2)40℃时,氯化钠的溶解度______(填“大于”、“小于”或“等于”)硝酸钾的溶解度。
(3)欲使硝酸钾的不饱和溶液转化为饱和溶液,可以采取的方法之一是 。
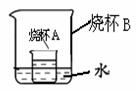
(4)如右图所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入生石灰后,烧杯A中变浑浊,可能的原因是______(填序号)。
A.反应消耗水,氢氧化钙析出
B.反应放热,温度升高,氢氧化钙溶解度降低
C.生石灰与水反应生成的氢氧化钙不再溶解
 |
(6分)根据表中内容回答下列问题。
|
|
0 |
20 |
40 |
60 |
80 |
||||||||||||||||||
|
KNO3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
||||||||||||||||||
|
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
||||||||||||||||||
|
Ca(OH)2 |
0.173 |
0.165 |
0.121 |
0.116 |
0.094 |
(1)随温度升高,硝酸钾溶解度的变化趋势是___ ____(填“增大”“减小”或“不变”)。
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是 ___ ____。
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100 g水中充分溶解,20℃时有如图1所示的实验现象,烧杯b中溶解的物质___ ____。
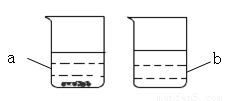
(4)如图2所示,若向烧杯中加入足量的硝酸铵使之充分溶解,可观察到的现象是___ ____。
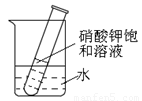
(5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是___ ____。
下表是3种物质在不同温度时的溶解度,根据表格信息答题.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
| Ca(OH)2 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 | |
(1)某饱和溶液随温度升高有固体析出,则该饱和溶液的溶质是 (填化学式).
(2)在60℃时,S(NaCl) S(KNO3)(填写“>”、“<”或“=”)。
(3)要配制20℃时的NaCl饱和溶液100g,需要N![]() aCl的质量为 g ;
aCl的质量为 g ;
(保留小数点后一位).
(4)某KNO3晶体中有少量NaCl杂质,要得到纯净KNO3的方法是:
先 ,然后 ![]() ,再过滤,洗涤、干燥后得到KNO3晶体.
,再过滤,洗涤、干燥后得到KNO3晶体.
(5)在盛有20℃时的Ca(OH)2 饱和溶液中,加入少量生石灰并待冷却至20℃。
与加入前相比,溶液中溶质的质量将 (填:增大、减小或不变),
溶液中溶质的质量分数将 (填:增大、减小或不变)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com