
题目列表(包括答案和解析)
已知25℃时CH3COOH和NH3?H2O的电离平衡常数分别为
![]() 。现有常温下1 mol/L的醋酸溶液和1 mol/L的氨水,且知醋酸溶液的pH=a,试回答下列问题:
。现有常温下1 mol/L的醋酸溶液和1 mol/L的氨水,且知醋酸溶液的pH=a,试回答下列问题:
(1)醋酸溶液中存在的电离平衡用电离方程式表示为:____________,在同样条件下,该浓度的氨水的pH=__________(用含a的代数式表达)。
(2)将上述两种溶液等体积混合,所得溶液的pH=___________。
(3)饱和氯化铵溶液显酸性,原因是___________;向饱和氯化铵溶液中加入少量Mg(OH)2固体,固体完全溶解,合理的解释用相关离子方程式表示为______________________
(4)向Mg(OH)2悬浊液中加入适量CH3COONH4溶液,Mg(OH)2能否完全溶解_______(填“能”或“否”),理由是____________________ 。
|
下列属于强电解质的是 ①NaOH ②NH3·H2O ③CaCO3 ④CH3COOH ⑤CH3COONH4 | |
| [ ] | |
A. |
①②③ |
B. |
②③④ |
C. |
①③⑤ |
D. |
①④⑤ |
下列说法中正确的是()。
A.CH3COOH与NaOH在相同条件下电离程度相等
B.NaCl晶体不能导电是因为其中有Na+和Cl-,但两者不能自由移动
C.H2SO4在电流作用下在水中电离出H+和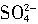
D.CH3COOH与NH3?H2O都是弱电解质,两者反应生成的CH3COONH4也是弱电解质
有等摩尔浓度的五种溶液: ① CH3COONa、 ② CH3COONH4、 ③ CH3COOH、 ④ NH3?H2O、 ⑤ NH4Cl。
(1)按溶液pH由大到小排列的顺序(写序号)为:
。
(2)按溶液中离子总浓度的大小关系排列顺序(写序号)为: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com