
题目列表(包括答案和解析)
A是有机羧酸盐,B、C、D是常见化合物; A、B、C、D焰色反应呈黄色,水溶液均呈碱性,其中B的碱性最强。X、Y是最常见的氧化物且与人体、生命息息相关,它们的晶体类型相同。A与B等物质的量反应生成D和一种气体单质;C受热分解得到Y、D和X;B与C反应生成D和X。E由两种元素组成,式量为83,将E投入X中得到B和气体Z,Z在标准状况下的密度为0.76g·L-1。
(1)A的化学式是??????? ????? 。Y的电子式是?????? ??????? 。
(2)X的沸点比同主族同类型物质要高,原因是? ???????????? ? 。
(3)写出E与足量盐酸反应的化学方程式???????????
(4)写出在D的饱和溶液中不断通Y析出C的离子方程式???????????? ?????? 。
(5)A的一个重要应用是根据2A →P +H2↑得到P,P溶液中的阴离子通常用CaCl2使之沉淀,当它完全沉淀时,溶液中Ca2+的物质的量浓度至少为????????? 。
(沉淀Ksp=2.3×10-9,当溶液中离子浓度≤10-5mol·L-1,即可认为完全沉淀)
(6)实验室常用P与足量HCl反应所得的有机物在浓硫酸条件下共热分解制某还原性气体,设计实验证明分解产物中还原性气体的存在?????????????????????????? 。
A是有机羧酸盐,B、C、D是常见化合物; A、B、C、D焰色反应呈黄色,水溶液均呈碱性,其中B的碱性最强。X、Y是最常见的氧化物且与人体、生命息息相关,它们的晶体类型相同。A与B等物质的量反应生成D和一种气体单质;C受热分解得到Y、D和X;B与C反应生成D和X。E由两种元素组成,式量为83,将E投入X中得到B和气体Z,Z在标准状况下的密度为0.76g·L-1。
(1)A的化学式是 。Y的电子式是 。
(2)X的沸点比同主族同类型物质要高,原因是 。
(3)写出E与足量盐酸反应的化学方程式
(4)写出在D的饱和溶液中不断通Y析出C的离子方程式 。
(5)A的一个重要应用是根据2A →P +H2↑得到P,P溶液中的阴离子通常用CaCl2使之沉淀,当它完全沉淀时,溶液中Ca2+的物质的量浓度至少为 。
(沉淀Ksp=2.3×10-9,当溶液中离子浓度≤10-5mol·L-1,即可认为完全沉淀)
(6)实验室常用P与足量HCl反应所得的有机物在浓硫酸条件下共热分解制某还原性气体,设计实验证明分解产物中还原性气体的存在 。
过渡金属元素及其化合物的应用研究是目前科学研究的前沿之一。试回答下列问题:
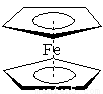
(1)二茂铁又叫双环戊二烯基铁[化学式:Fe(C5H5)2],结构如图所示,是一种具有芳香族性质的有机金属化合物。外观为橙色,熔点为172℃,沸点249℃,100℃以上能升华;不溶于水,溶于甲醇、乙醇等有机溶剂中。基态Fe2+离子的电子排布式为 。1 mol环戊二烯中含有的σ键的数目是 。
(2)铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是 。
|
电离能/kJ·mol-1 |
I1 |
I2 |
|
铜 |
746 |
1958 |
|
锌 |
906 |
1733 |
(3)现有含钛的两种颜色的晶体,Ti3+的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的2/3。
试推断紫色晶体的化学式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com