
题目列表(包括答案和解析)
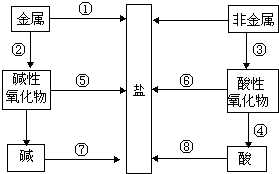 单质、氧化物、酸、碱和盐的相互关系,可以用如图简单表示.请按要求图中每个指定序号的转变用一个相应的化学方程式表示.
单质、氧化物、酸、碱和盐的相互关系,可以用如图简单表示.请按要求图中每个指定序号的转变用一个相应的化学方程式表示.
| ||
| ||
| ||
| ||
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动。探究l:研究常见的物质一一氢氧化钠和盐酸的反应程度。
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 固体化台物________。 | | 盐酸过量 |
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 固体化台物______. | ______ | 盐酸过量 |
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动。探究l:研究常见的物质一一氢氧化钠和盐酸的反应程度。
|
实验内容 |
实验现象 |
解释与结论 |
|
取反应后少量溶液于试管中,加入 固体化台物________。 |
|
盐酸过量
|
探究2:研究酸的性质----硫酸、盐酸和锌反应
通过探究实验,同学们发现硫酸和盐酸溶液都可以和锌反应产生氢气。产生这种共同现象的原因为
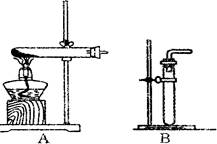
探究3:探索未知一一浓硝酸和铜制取气体。
已知Cu十4HN03(浓)=Cu( NO3)2+H2O+2N02↑ 。N02能和水反应生成硝酸和N0。NO和NO2都是空气的污染物。
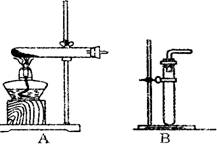
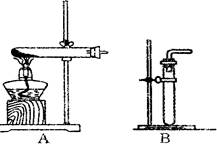
(1)利用该反应制取二氧化氮的发生装置,应选用图所示装置中的_______。收集N02的方法为________ 。
(2)反应NO+X→N02中,X的化学式应为____;若用浓硝酸和铜制取NO,应采用的收集方法是____
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入l0g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009. 8g,请你计算所加碳酸钠溶液的溶质质量分数?
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 固体化台物________。 | | 盐酸过量 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com