
题目列表(包括答案和解析)
下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有第ⅥA族和几种元素的位置。请回答下列问题:
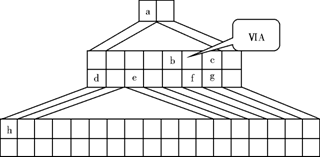
(1)请在上图中将铁元素所在族的位置全部涂黑。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是:氢的最外层电子“饱和缺一”。请写出NaH的电子式 。
(3)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,土壤中施用该盐做化肥时,其阴离子在水田中的利用率低,说明土壤胶体粒子带 (“正”或“负”)电荷。
(4)下列叙述正确的是 。
A.h的最高价氧化物对应的水化物是一种强碱
B.硒化氢的稳定性强于f的氢化物的稳定性
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>a
E.相同条件下,d与f形成的化合物水溶液的pH大于d与g形成的化合物水溶液的pH,说明相同浓度氢化物水溶液的酸性f弱于g
(5)d的某化合物呈淡黄色,可与氯化亚铁溶液反应生成红褐色沉淀和能使带火星的木条复燃的气体,若沉淀和气体的物质的量之比为2∶1,反应的离子方程式为 。
(14分)下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有ⅥA族和几种元素的位置。请回答下列问题:
(1)g元素在周期表中的位置 。元素a和w形成的化合物wa3是 分子(填”极性”或”非极性”)。
(2)d的氢化物的沸点比h的氢化物的沸点 ,(填”高”、”低”或”相等”)原因是 。
(3)用电子式表示化合物eh的形成过程 。
(4)b和w可形成一种原子晶体,它的用途有 ,(答一种即可)由化合物b(wa2)4在高温下分解可生成wa,和该原子晶体。则该原子晶体的化学式为 。
(14分)下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有ⅥA族和几种元素的位置。请回答下列问题: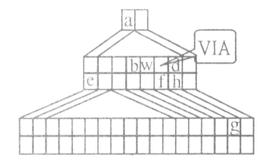
(1)g元素在周期表中的位置 。元素a和w形成的化合物wa3是 分子(填 ”极性”或”非极性”)。
”极性”或”非极性”)。
(2)d的氢 化物的沸点比h的氢
化物的沸点比h的氢 化物的沸点 ,(填”高”、”低”或”相等”)原因是 。
化物的沸点 ,(填”高”、”低”或”相等”)原因是 。
(3)用电子式表示化合物eh的形成过程 。
(4)b和w可形成一种原子晶体,它的用途有 ,(答一种即 可)由化合物b(wa2)4在高温下分解可生成wa,和该原子晶体。则该原子晶体的化学式为 。
可)由化合物b(wa2)4在高温下分解可生成wa,和该原子晶体。则该原子晶体的化学式为 。
下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有第ⅥA族和几种元素的位置。请回答下列问题: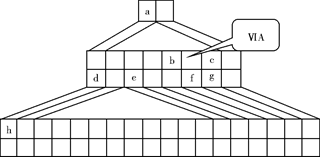
(1)请在上图中将铁元素所在族的位置全部涂黑。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是:氢的最外层电子“饱和缺一”。请写出NaH的电子式 。
(3)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,土壤中施用该盐做化肥时,其阴离子在水田中的利用率低,说明土壤胶体粒子带 (“正”或“负”)电荷。
(4)下列叙述正确的是 。
| A.h的最高价氧化物对应的水化物是一种强碱 |
| B.硒化氢的稳定性强于f的氢化物的稳定性 |
| C.c的氢化物的水溶液是强酸 |
| D.原子半径:h>e>a |
(14分)下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有ⅥA族和几种元素的位置。请回答下列问题:
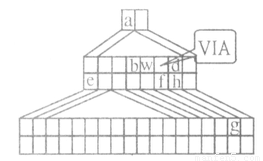
(1)g元素在周期表中的位置 。元素a和w形成的化合物wa3是 分子(填”极性”或”非极性”)。
(2)d的氢化物的沸点比h的氢化物的沸点 ,(填”高”、”低”或”相等”)原因是 。
(3)用电子式表示化合物eh的形成过程 。
(4)b和w可形成一种原子晶体,它的用途有 ,(答一种即可)由化合物b(wa2)4在高温下分解可生成wa,和该原子晶体。则该原子晶体的化学式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com