
题目列表(包括答案和解析)
(16分)(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示):
;
实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈 性 ,原因是(用离子方程式表示):__________________
_ ____________________ _____________________________ 。
____________________ _____________________________ 。
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
(16分)
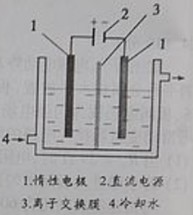
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。请回答下列问题:
(1)碘是 (填颜色)固体物质,实验室常用 方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为 ;阴极上观察到的实验现象是 。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I—。请设计一个检验电解液中是否有I—的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。

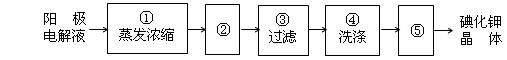
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:

步骤②的操作名称是 ,步骤⑤的操作名称是 。步骤④洗涤晶体的目的是 。
(16分)碘被称为“智力元素”,科学合理地补碘可防止点缺乏症。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如有图所示。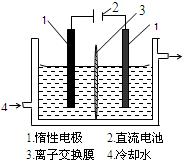
请回答下列问题:
(1)碘是___(填颜色)固体物质,实验室常用____方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I2 + 6KOH =" 5KI" + KIO3 + 3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为________________________;阴极上观察到的实验现象是______________________________。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解液中是否有I-的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。
| 实验方法 | 实验现象及结论 |
| | |
(16分)工业“从海水中提取镁”的流程图如下:
步骤为:
①将海边大量的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
②将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
③在Mg(OH)2沉淀中加入盐酸得到MgCI2溶液,再经蒸发结晶得到MgCl2·6H2O;
④将MgCl2·6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的氯化镁可得到Mg。
⑴步骤①中涉及的化学方程式为 。
⑵步骤③中的蒸发利用风吹日晒完成,但在实验室中蒸发操作时需要的主要仪器有 、 、酒精灯、三脚架、泥三角、坩埚钳等。
⑶海水中的镁以Mg2+形式存在,设计步骤②③将Mg2+转化为Mg(OH)2又重新转化为Mg2+的目的是 。
⑷步骤④中的“一定条件”指的是 ,目的是 。
⑸上述流程中,在降低成本、减少污染方面做了一些工作,请写出其中一点:
⑹有同学认为:可以在步骤②后加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,以简化实验步骤,体现实验的简约性原则。你是否同意该同学的观点 (填“同意”或“不同意”),理由为 。
(16分)某学习小组以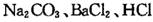 溶液作试剂,设计提纯含有少量
溶液作试剂,设计提纯含有少量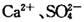 的粗盐。其实验方案如下:
的粗盐。其实验方案如下:
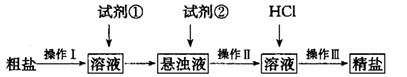
(1) 操作I的名称为________;试剂①应选用_______;检验试剂②是否过量的方法______。
(2) 操作I〜III共用到玻璃棒________次;从悬浊液到精盐的实验过程中,某同学未按上述方案进行,最终导致精盐纯度偏低。其做法可能是________________。
(3)测定产品精盐中NaCl的含量的实验步骤是:
第一步:准确称取a g干燥精盐于锥形瓶中,加人30. OmL蒸馏水。
第二步:向上述锥形瓶中加人几滴突光素指示剂。
第三步:用浓度为的AgNO3标液滴至终点(溶液呈浅红色),消耗AgNO3溶液V mL。
①盛装干燥精盐的烧杯应放在________中保存(填仪器名称);
②终点时溶液呈浅红色是荧光素指示剂与________反应(填“Ag+”或"NO3-”);
③某同学在第二次滴定时,滴定前,后管内液面分别如图,则其所得V=________mL;
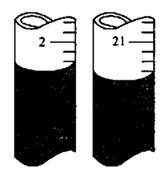
④NaCl的质量分数为________ (用字母表示)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com