
题目列表(包括答案和解析)
为测定某工厂烟道气中SO2的含量,使16.00L烟道气缓慢通过1L水,设SO2完全被吸收,且溶液体积不改变。取出其中20.00mL溶液,加入2—3滴淀粉溶液后,用1.18×10-3mol/L的饱和碘水(密度为1g/cm3)滴定,耗去19.07mL达到终点。(反应为SO2+I2+2H2O→H2SO4+2HI)求
(1)实验条件下碘的溶解度;
(2)该厂烟道气中SO2的含量(mg/L);
(3)为简便计算,在其余操作都不变的情况下,要使滴定时每水泵5mL碘水相当于烟道气中含SO21mg./L,则所配制的碘水的物质的量浓度为多少?
形成酸雨的原理之一可简示如下;
含硫燃料 ![]() A→B→硫酸。
A→B→硫酸。
回答下列问题:
(1)A物质的化学式是________,B物质的化学式是________。
(2)三个反应中不属于氧化还原反应的是________。
(3)SO2中硫元素显+4价,它可能降低到0价,利用这一性质可在工厂的烟道气中通入合适的________(填“氧化剂”或“还原剂”),除去SO2气体,达到减小污染的目的。
(4)从环境保护的角度,雨水的pH<5.6时就判断为酸雨。经测定某次雨水中只含硫酸,且浓度为1×10-5mo1·L-1,则这次降雨________(填“是”或“不是”)酸雨。
(5)火力发电厂燃烧的煤中含有大量的硫,其排出的废气中往往含有SO2、O2、N2、CO2等。为了除去有害的SO2气体,在英国已进行的一个研究结果表明;高烟囱可以有效降低地表面SO2浓度。在20世纪60年代到70年代的10年间,由发电厂排放的SO2增加了35%,但由于建造高烟囱的结果,SO2地面浓度降低了30%之多。
Ⅰ.你认为减少酸雨产生的途径可采取的措施是________。
A. 少用煤作燃料 B. 把工厂烟囱造高 C. 燃料脱硫 D. 把工厂迁移到农村 E. 开发新能源
Ⅱ.请从全球环境保护的角度,分析这种建造高烟囱的方法是否可取________,理由是_____________________________________________________。
含硫燃料 ![]() A→B→硫酸。
A→B→硫酸。
回答下列问题:
(1)A物质的化学式是________,B物质的化学式是________。
(2)三个反应中不属于氧化还原反应的是________。
(3)SO2中硫元素显+4价,它可能降低到0价,利用这一性质可在工厂的烟道气中通入合适的________(填“氧化剂”或“还原剂”),除去SO2气体,达到减小污染的目的。
(4)从环境保护的角度,雨水的pH<5.6时就判断为酸雨。经测定某次雨水中只含硫酸,且浓度为1×10-5mo1·L-1,则这次降雨________(填“是”或“不是”)酸雨。
(5)火力发电厂燃烧的煤中含有大量的硫,其排出的废气中往往含有SO2、O2、N2、CO2等。为了除去有害的SO2气体,在英国已进行的一个研究结果表明;高烟囱可以有效降低地表面SO2浓度。在20世纪60年代到70年代的10年间,由发电厂排放的SO2增加了35%,但由于建造高烟囱的结果,SO2地面浓度降低了30%之多。
Ⅰ.你认为减少酸雨产生的途径可采取的措施是________。
A. 少用煤作燃料 B. 把工厂烟囱造高 C. 燃料脱硫 D. 把工厂迁移到农村 E. 开发新能源
Ⅱ.请从全球环境保护的角度,分析这种建造高烟囱的方法是否可取________,理由是_____________________________________________________。
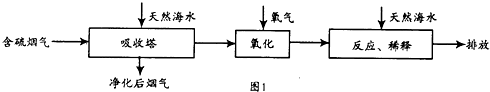
| 实验序号 | 温度(K) | 含硫烟气SO2浓度(10-6mol.l-1) | 脱硫率(%) |
| Ⅰ | 298 | 400 | 99.5 |
| Ⅱ | T | 500 | 97.1 |
| Ⅲ | 313 | 400 | 94.3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com