
题目列表(包括答案和解析)
(1)若向氨水中加入少量硫酸铵固体,此时溶液中![]() ____________(填“增大”“减小”或“不变”)。
____________(填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式__________________;所得溶液的pH____________7(填“>”“<”或“=”),用离子方程式表示其原因______________
_____________________________________________________________________。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(![]() )=a mol·L-1,则c(
)=a mol·L-1,则c(![]() )=_______。
)=_______。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的顺序是______________________________________________________。
现有25 ℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 _________(填“增大”“减小”或“不变”)。
_________(填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式____________________;所得溶液的pH___ 7(填“<”“>”或“=”),用离子方程式表示其原因_________________。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH )=a mol/L,则c(SO
)=a mol/L,则c(SO )=__________。
)=__________。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的顺序是___ _______。
现有25 ℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中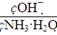 _________(填“增大”“减小”或“不变”)。
_________(填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式____________________;所得溶液的pH___ 7(填“<”“>”或“=”),用离子方程式表示其原因_________________。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH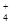 )=a mol/L,则c(SO
)=a mol/L,则c(SO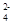 )=__________。
)=__________。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的顺序是___ _______。
| [OH-] |
| [NH3?H2O] |
| +4 |
| 2-4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com