
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
 2NH3 (g)¡£̉ÑÖª¼ÓÈë1mol N2ºÍ3mol H2£¬ÔÚºăѹ̀ơ¼₫Ï£¬´ïµ½Æ½ºâʱÉú³Éamol NH3¡£[¼ûϱíÖбàºÅ(1)µÄ̉»ĐĐ]£»ÔÚºăÈỪơ¼₫Ï£¬´ïµ½Æ½ºâʱÉú³É
2NH3 (g)¡£̉ÑÖª¼ÓÈë1mol N2ºÍ3mol H2£¬ÔÚºăѹ̀ơ¼₫Ï£¬´ïµ½Æ½ºâʱÉú³Éamol NH3¡£[¼ûϱíÖбàºÅ(1)µÄ̉»ĐĐ]£»ÔÚºăÈỪơ¼₫Ï£¬´ïµ½Æ½ºâʱÉú³É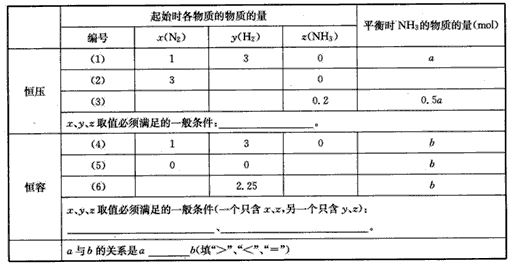
£¨14·Ö£©ĂܱƠÈƯÆ÷ÖĐ£¬±£³Ö̉»¶¨Î¶ȣ¬½øĐĐÈçÏ·´Ó¦£ºN2£¨g£©£«3H2£¨g£©![]() 2NH3£¨g£©¡£
2NH3£¨g£©¡£
̉ÑÖª¼ÓÈë1mol N2ºÍ3mol H2£¬ÔÚºăѹ̀ơ¼₫Ï£¬´ïµ½Æ½ºâʱÉú³Éamol NH3[¼ûϱíÖбàºÅ£¨1£©µÄ̉»ĐĐ]£»ÔÚºăÈỪơ¼₫Ï£¬´ïµ½Æ½ºâʱÉú³Éb mol NH3[¼ûϱíÖбàºÅ£¨4£©µÄ̉»ĐĐ]¡£ÈôÏàͬ̀ơ¼₫Ï£¬´ïµ½Æ½ºâʱ»́ºÏÎïÖи÷×é·ÖµÄ°Ù·Öº¬Á¿²»±ä£¬Çë̀î¿Ơ£º![]()
×´×´ ̀ơ¼₫ | Æđʼʱ¸÷ÎïµÄÎïÖʵÄÁ¿£¨mol£© | ƽºâʱNH3µÄÎïÖʵÄÁ¿ £¨mol£© | ||||
±àºÅ | x£¨N2£© | y£¨H2£© | z£¨NH3£© | |||
ºă
ѹ | £¨1£© | 1 | 3 | 0 | a | |
£¨2£© | 3 |
| 0 |
| ||
£¨3£© |
|
| 0.2 | 0.5a | ||
x¡¢y¡¢zÈ¡Öµ±ØĐëÂú×ăµÄ̉»°ằơ¼₫£º ¡£ | ||||||
ºă
ÈƯ | £¨4£© | 1 | 3 | 0 | b | |
£¨5£© | 0 | 0 |
| b | ||
£¨6£© |
| 2.25 |
| b | ||
x¡¢y¡¢zÈ¡Öµ±ØĐëÂú×ẳ»°ằơ¼₫£¨̉»¸öÖ»º¬x¡¢z£¬Áí̉»¸öÖ»º¬y¡¢z£©£º £» ¡£ | ||||||
| aÓëbµÄ¹ØϵÊÇ£ºa b£῭¡¢£¼¡¢£½£© | |||||
| 27 |
| 16 |
| 27 |
| 16 |
| [NH3]2 |
| [N2][H2]3 |
| [NH3]2 |
| [N2][H2]3 |
| ×´̀¬ ̀ơ¼₫ |
ÆđʼʱÎïÖʵÄÎïÖʵÄÁ¿£¨mol£© | ƽºâʱNH3µÄÎïÖʵÄÁ¿£¨mol£© | |||
| ±àºÅ | X£¨N2£© | Y£¨H2£© | Z£¨NH3£© | ||
| ºăѹ | ¢Ù | 1 | 3 | 0 | a |
| ¢Ú | 2.25 | a | |||
| ¢Û | 2 | 3a | |||
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com