
题目列表(包括答案和解析)


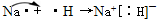
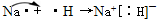




下表是元素周期表的一部分.表中所列的字母分别代表某一化学元素.
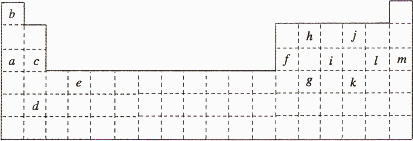
(1)①请用粗实线在上图中画出金属元素与非金属元素的分界线.
②写出g元素在周期表中的位置:________________.
(2)下列________(填写编号)组元素的单质可能都是电的良导体.
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(3)现有下列短周期元素性质的数据:
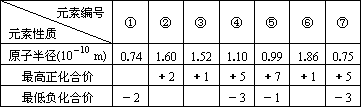
试回答下列问题:
Ⅰ.上述元素中①、②、⑥分别为________,上述元素中处于第二周期的有________(以上均用元素符号表示).
Ⅱ.元素④与元素⑦相比较,气态氢化物较稳定的是________(填化学式).
Ⅲ.工业上主要获取⑤的单质的化学反应方程式为:________.
Ⅳ.⑤和⑥形成的化合物中化学键是________________.
某短周期元素A,其最高价氧化物对应水化物甲与其气态氢化物乙反应可生成盐丙。已知乙的密度是同温同压下H?2密度的8.5倍。
请回答:
(1)乙的电子式为 。
(2)甲具有不稳定性,其发生分解的化学反应方程式为 。
实验室保存甲的方法是 。
(3)在一定条件下,将乙放入固定容积的密闭容器中使其发生分解反应,已知△H>0,达到平衡状态后,改变其中一个条件X,Y随X的变化符合图中曲线的是
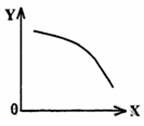 (选填字母)
(选填字母)
a.当X表示温度时,Y表示乙的物质的量
b.当X表示压强时,Y表示乙的转化率
c.当X表示反应时间时,Y表示混合气体的密度
d.当X表示乙的物质的量时,Y表示某一生成物的物质的量
(4)现有硫酸甲的混合液20mL,其中硫酸的物质的量浓度为2mol?L―1,甲的物质的量浓度为1mol?L-1。向该混合液中加入0.96g铜粉,假设只生成一种无色气体,则所收集到的气体的体积在标准状况下为 。
(5)丙对水的电离起 作用(填“抑制”、“促进”或“不影响”),原因是(结合离子方程式简要说明) 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |

| M | ||
4
|
| M | ||
4
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com