
题目列表(包括答案和解析)
实验室可用环己醇(沸点:160.84℃,微溶于水)制备环己酮(沸点:155.6℃,微溶于水),使用的氧化剂可以是次氯酸钠、重铬酸钾等。

下列装置分别是产品的合成装置和精制装置示意图:

合成实验过程如下:
向装有搅拌器、滴液漏斗和温度计的三颈烧瓶中依次加入5.2 mL环己醇和25 mL冰醋酸。开动搅拌器,将40 mL次氯酸钠溶液逐渐加入到反应瓶中,并使瓶内温度维持在30~35℃,用磁性搅拌器搅拌5 min。然后,在室温下继续搅拌30 min后,在合成装置中再加入30 mL水、3g氯化铝和几粒沸石,加热蒸馏至馏出液无油珠滴出为止。
回答下列问题:
(1)在合成装置中,甲装置的名称是 。
(2)三颈烧瓶的容量为 (填“50 mL"、“100 mL”或“250 mL")。
(3)滴液漏斗具有特殊的结构,主要目的是____ 。
(4)蒸馏完成后,向馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是 。然后加入精制食盐使之变成饱和溶液,将混合液倒人____ 中,分离得到有机层。
(5)用如上右图对粗产品进行精制,蒸馏收集____ ℃的馏分。
(6)检验坏己酮是否纯净,可使用的试剂为____ 。
A.重铬酸钾溶液 B.金属钠 C.新制的氢氧化铜悬浊液
药品:①2% NaOH溶液②稀HCl③稀H![]() SO
SO![]() ④饱和KHCO
④饱和KHCO![]() 溶液⑤浓H
溶液⑤浓H![]() SO
SO![]() ⑥CaCO
⑥CaCO![]() 固体⑦K
固体⑦K![]() CO
CO![]() 粉末
粉末
仪器装置(如图所示):
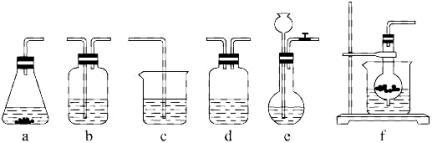
请根据题目要求完成下列问题:
请按下表要求,填写选择的装置和药品。
分项内容 | CO | 除杂洗气装置(Y) | 制备产品装置(Z) |
选择的装置 (填序号) |
|
| C |
选择的药品 (填序号) |
|
| ① |
(2)如何检验所选择的CO![]() 发生装置(X)的气密性,请写出主要操作过程:__________。
发生装置(X)的气密性,请写出主要操作过程:__________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为_____________,Y装置中除去的杂质为_________________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是______________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过________________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
化学式 | Na | NaHCO | NaOH | NaCl | Na |
溶解度 (g/100 g H | 21.3 | 9.60 | 107 | 35.8 | 19.4
|
某校化学研究性学习小组利用下面所提供的仪器装置和药品制取NaHCO![]() 溶液,设计如下实验。实验室提供的药品、仪器装置如下:
溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2% NaOH溶液②稀HCl③稀H![]() SO
SO![]() ④饱和KHCO
④饱和KHCO![]() 溶液⑤浓H
溶液⑤浓H![]() SO
SO![]() ⑥CaCO
⑥CaCO![]() 固体⑦K
固体⑦K![]() CO
CO![]() 粉末
粉末
仪器装置(如图所示):
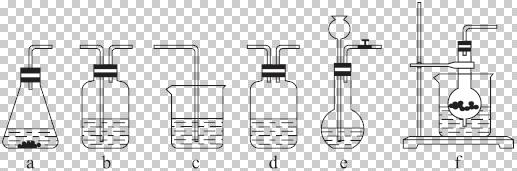
请根据题目要求完成下列问题:
请按下表要求,填写选择的装置和药品。
| 分项 内容 | CO (随开随用,随关随停) (X) | 除杂洗 气装置 (Y) | 制备产 品装置 (Z) |
| 选择的装置 (填序号) | C | ||
| 选择的药品 (填序号) | ① |
(2)如何检验所选择的CO![]() 发生装置(X)的气密性,请写出主要操作过程:__________。
发生装置(X)的气密性,请写出主要操作过程:__________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为_____________,Y装置中除去的杂质为_________________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是______________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过________________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
| 化学式 | Na | NaHCO | NaOH | NaCl | Na |
| 溶解度 (g/100 g H | 21.3 | 9.60 | 107 | 35.8 | 19.4 |
(10分)下表是稀硫酸与金属镁反应的实验数据:
|
实验 序号 |
金属质量/g |
金属 状态 |
c(H2SO4) /mol/L |
V(H2SO4)/mL |
溶液温度/℃ |
金属消失 的时间/s |
|
|
反应前 |
反应后 |
||||||
|
1 |
0.24 |
丝 |
0.5 |
100 |
20 |
34 |
500 |
|
2 |
0.24 |
粉末 |
0.5 |
100 |
20 |
35 |
50 |
|
3 |
0.24 |
丝 |
0.7 |
100 |
20 |
36 |
250 |
|
4 |
0.24 |
丝 |
0.8 |
100 |
20 |
35 |
200 |
|
5 |
0.24 |
粉末 |
0.8 |
100 |
20 |
36 |
25 |
|
6 |
0.24 |
丝 |
1.0 |
100 |
20 |
35 |
125 |
|
7 |
0.24 |
丝 |
1.0 |
100 |
35 |
50 |
50 |
|
8 |
0.24 |
丝 |
1.1 |
100 |
20 |
34 |
100 |
|
9 |
0.24 |
丝 |
1.1 |
100 |
30 |
44 |
40 |
分析上述数据,回答下列问题:
(1)实验4和5表明, 对反应速率有影响, 反应速率越快,能表明同一规律的实验还有 (填实验序号);
(2)其中仅表明反应物浓度对反应速率产生影响是实验2和实验 (填实验序号);
(3)本实验中影响反应速率的其他因素还有 ____ ,能表明这一规律的分别是实验6和实验 或实验8和实验 ;(填实验序号);
(4)实验中的所有反应,反应速率最快是实验 (填实验序号),该实验中硫酸平均反应速率为 ;
某校化学研究性学习小组利用下面所提供的仪器装置和药品制取NaHCO3溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2% NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3固体 ⑦K2CO3粉末
仪器装置(如图所示):
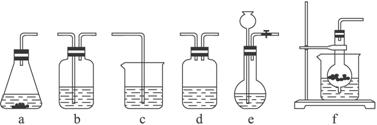
请根据题目要求完成下列问题:
(1)请按下表要求,填写选择的装置和药品。
| 分项 内容 | CO2发生装置(随开随用,随关随停)(X) | 除杂洗气装置(Y) | 制备产品装置(Z) |
| 选择的装置(填序号) | c | ||
| 选择的药品(填序号) | ① |
(2)如何检验所选择的CO2发生装置(X)的气密性,请写出主要操作过程:_________________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为________________________,Y装置中除去的杂质为_____________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是____________________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过_______________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
| 化学式 | Na2CO3 | NaHCO3 | NaOH | NaCl | Na2SO4 |
| 溶解度(g/100 g H2O) | 21.3 | 9.60 | 107 | 35.8 | 19.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com