(14·Ö)(1)½ðÊôÄø¼°Æ仯ºÏÎïÔںϽð²ÄÁÏÒÔ¼°´ß»¯¼ÁµÈ·½ÃæÓ¦Óù㷺¡£Çë»Ø´ðÏÂÁÐÎÊÌ⣺
¢ÙNiO¡¢FeOµÄ¾§Ìå½á¹¹ÀàÐ;ùÓëÂÈ»¯ÄƵÄÏàͬ£¬Ni
2£«ºÍFe
2£«µÄÀë×Ӱ뾶·Ö±ðΪ69 pmºÍ78 pm£¬ÔòÈÛµãFeO
NiO (Ìî¡°£¼¡±»ò¡°£¾¡±)£»
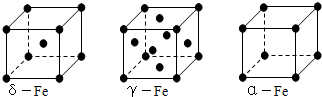
¢ÚÌúÓЦġ¢¦Ã¡¢¦ÁÈýÖÖͬËØÒìÐÎÌ壬¸÷¾§°ûÈçÏÂͼ£¬Ôò¦Ä¡¢¦ÁÁ½ÖÖ¾§°ûÖÐÌúÔ×ÓµÄÅäλÊýÖ®±ÈΪ
¡£
(2)ÔªËؽð(Au)´¦ÓÚÖÜÆÚ±íÖеĵÚÁùÖÜÆÚ£¬ÓëCuͬ×壬һÖÖͽðºÏ½ð¾§Ìå¾ßÓÐÁ¢·½×îÃܶѻýµÄ½á¹¹£¬ÔÚ¾§°ûÖÐCuÔ×Ó´¦ÓÚÃæÐÄ£¬AuÔ×Ó´¦ÓÚ¶¥µãλÖã¬Ôò¸ÃºÏ½ðÖÐCuÔ×ÓÓëAuÔ×ÓÊýÁ¿Ö®±ÈΪ
£»¸Ã¾§ÌåÖУ¬Ô×ÓÖ®¼äµÄÇ¿Ï໥×÷ÓÃÊÇ
£»
£¨3£©2007Äêŵ±´¶ûÎïÀíѧ½±Îª·¨¹ú¿Æѧ¼Ò°¢¶û±´¡¤·Ñ¶ûºÍµÂ¹ú¿Æѧ¼Ò±ËµÃ¡¤¸ñÁÖ±´¸ñ¶û¹²Í¬»ñµÃ£¬ÒÔ±íÕÃËûÃÇÔھ޴ŵç×èЧӦ(CMRЧӦ)Ñо¿·½ÃæµÄ³É¾Í¡£Ä³¸ÆîÑÐ͸´ºÏÑõ»¯ÎïÈçͼËùʾ£¬ÒÔAÔ×ÓΪ¾§°ûµÄ¶¥µã£¬Aλ¿ÉÒÔÊÇCa¡¢Sr¡¢Ba»òPb£¬µ±BλÊÇV¡¢Cr¡¢Mn¡¢FeµÈʱ£¬ÕâÖÖ»¯ºÏÎï¾ßÓÐCMRЧӦ¡£
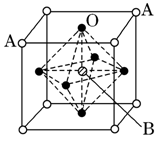
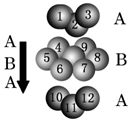
¢ÙÓÃA¡¢B¡¢O±íʾÕâÀàÌØÊ⾧ÌåµÄ»¯Ñ§Ê½£º
¡£
¢ÚÒÑÖªLaΪ£«3¼Û£¬µ±±»¸ÆµÈ¶þ¼ÛÔªËØAÌæ´úʱ£¬¿ÉÐγɸ´ºÏ¸Æîѿ󻯺ÏÎïLa
1£xA
xMnO
3(x<0.1)£¬´Ëʱһ²¿·ÖÃÌת±äΪ£«4¼Û¡£µ¼Ö²ÄÁÏÔÚijһζȸ½½üÓз´Ìú´Å¡ªÌú´Å¡¢Ìú´Å¡ªË³´Å¼°½ðÊô¡ª°ëµ¼ÌåµÄת±ä£¬ÔòLa
1£xA
xMnO
3ÖÐÈý¼ÛÃÌÓëËļÛÃ̵ÄÎïÖʵÄÁ¿Ö®±ÈΪ£º
¡£
¢ÛÏÂÁÐÓйØ˵·¨ÕýÈ·µÄÊÇ
¡£
A£®ïç¡¢ÃÌ¡¢Ñõ·Ö±ðλÓÚÖÜÆÚ±íf¡¢d¡¢pÇø
B£®ÑõµÄµÚÒ»µçÀëÄܱȵªµÄµÚÒ»µçÀëÄÜ´ó
C£®Ã̵ĵ縺ÐÔΪ1.59£¬CrµÄµç¸ºÐÔΪ1.66£¬ËµÃ÷Ã̵ĽðÊôÐԱȸõÇ¿
D£®¸õµÄ¶Ñ»ý·½Ê½Óë¼ØÏàͬ£¬ÔòÆä¶Ñ»ý·½Ê½ÈçͼËùʾ



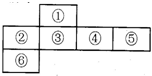 ¶ÌÖÜÆÚÔªËØÖУ¬Ä³Ð©²»Í¬×åÔªËصĵ¥Öʼ°Æ仯ºÏÎïÓÐÏàËƵĻ¯Ñ§ÐÔÖÊ£¬ÈçîëºÍÂÁ¶¼ÄÜÓëÇâÑõ»¯ÄÆÈÜÒº·´Ó¦£»ÈçͼÊÇÔªËØÖÜÆÚ±íµÄÒ»²¿·Ö£¬±àºÅΪ¢ÛµÄÔªËØ×îÍâ²ãÓë×îÄÚ²ãµç×ÓÊýÏàµÈ
¶ÌÖÜÆÚÔªËØÖУ¬Ä³Ð©²»Í¬×åÔªËصĵ¥Öʼ°Æ仯ºÏÎïÓÐÏàËƵĻ¯Ñ§ÐÔÖÊ£¬ÈçîëºÍÂÁ¶¼ÄÜÓëÇâÑõ»¯ÄÆÈÜÒº·´Ó¦£»ÈçͼÊÇÔªËØÖÜÆÚ±íµÄÒ»²¿·Ö£¬±àºÅΪ¢ÛµÄÔªËØ×îÍâ²ãÓë×îÄÚ²ãµç×ÓÊýÏàµÈ




