
题目列表(包括答案和解析)
化学式为C11H12O4的芳香族化合物A、B互为同分异构体,A和D都能发生银镜反应,E的一溴取代物只有两种, A经①、②两步反应得C、D和E。B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如图所示。
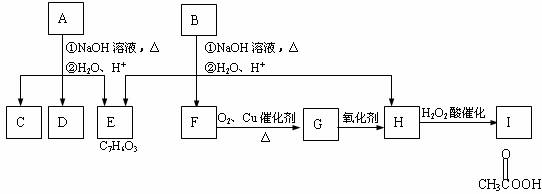
(1)A有2种可能结构,写出其结构简式 。
(2)在B、C、D、F、G、I化合物中,互为同系物的是 。
(3)写出D与F在加热和浓H2SO4催化作用下发生反应的化学方程式 ,指出反应类型 。
(4)除银镜反应外至少选用其它两种实验方法证明D具有还原性,请按要求填写下表:
| 所选试剂 | 观察到的实验现象 | |
| 方法1 | ||
| 方法2 |
A方案:加热条件下NH3还原CuO制得纯净的N2和活性铜粉
B方案:加热NaNO2和NH4Cl的浓溶液制得N2
C方案:将空气缓慢地通过灼热的铜粉制得较纯的N2
现实验室有可供选择的如下几种仪器用来制取N2
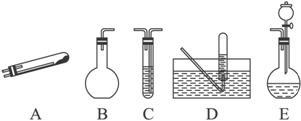
(1)若按A方案制N2时需要的氨气用生石灰和浓氨水作原料制取,则宜采用上述仪器中的___________(填编号)作NH3的发生器,该发生装置中发生的化学反应方程式为______________。要制取并收集纯净的N2(允许含有少量水蒸气),还须使用上述仪器中的(按气流从左到右的流向顺序列出)___________(填编号)。
(2)若按C方案制N2,空气是在加入__________(填物质的化学式)以后,通过仪器__________(填编号),将空气送入反应器的。反应器内可观察到的现象是______________。
(3)上述制N2的三个方案中,A、C两方案结合使用越来越受到人们的关注,这种方法和B方案相比,其优越性在于____________________________。
 化学是一门以实验为基础的自然科学,
化学是一门以实验为基础的自然科学,
化学实验在化学学习中具有重要的作用。
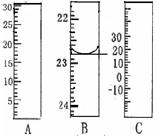
右图分别是温度计、量筒、滴定管的一部分,
其中A仪器的名称为 ,
B的正确读数为 。
(2)实验室很难配制准确浓度的NaOH溶液,需要
![]() 用基准物质来标定,邻苯二甲酸氢钾( ,,相对分子质量为204.0)是常用的基准物质。某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度。在本实验中达到滴定终点时,溶液的pH约为9.1。
用基准物质来标定,邻苯二甲酸氢钾( ,,相对分子质量为204.0)是常用的基准物质。某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度。在本实验中达到滴定终点时,溶液的pH约为9.1。
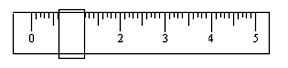 ①该学生用托盘天平称量时,先在两边托盘上放等质量的纸片,取少量邻苯二甲酸氢钾置于左盘,只用游码(单位:g)调整平衡时如下图所示。由此可知,所取邻苯二甲酸氢钾的质量为 g。
①该学生用托盘天平称量时,先在两边托盘上放等质量的纸片,取少量邻苯二甲酸氢钾置于左盘,只用游码(单位:g)调整平衡时如下图所示。由此可知,所取邻苯二甲酸氢钾的质量为 g。
②将称好的邻苯二甲酸氢钾置于锥形瓶中,加适量蒸馏水完全溶解得到无色溶液,再加入1~2滴 指示剂,当观察到 现象时,可停止滴定,记录数据。
③该学生进行了三次实验,所取固体质量均相同,达到滴定终点时记录所用未知氢氧化钠溶液的体积如下表:
| 实验编号 | NaOH溶液的体积(mL) |
| 1 | 22.52 |
| 2 | 22.49 |
| 3 | 22.50 |
则计算氢氧化钠溶液物质的量浓度的表达式为: (用数据表示,不需计算)
④以下操作会造成NaOH溶液浓度偏高的是 (填序号)
A.未用氢氧化钠溶液洗涤碱式滴定管
B.滴定前平视,滴定后俯视读数
C.滴定前滴定管尖嘴有气泡,滴定后气泡消失
D.滴定前未用邻苯二甲酸氢钾溶液洗锥形瓶
化学活动课上,三组学生分别用图示甲、乙两装置,探究“NaHCO3,和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查)。

请回答:
(1)各组反应开始时_____________,装置中的气球体积先变大,该装置中反应的离子方程式是_________________________。
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格。
| 试剂用量 | 实验现象 | 分析原因 | |
| 第①组 | 0.42 g NaHCO3 0.53 g Na2CO3 3 mL 4 mol / L盐酸 | 甲中气球与乙中气球的体积相等 | 甲、乙盐酸均过量 n(NaHCO3)=n(Na2CO3) V甲(CO2)= V乙(CO2) |
| 第②组 | 0.3 g NaHCO3 0.3 g Na2CO3 3 mL 4 mol / L盐酸 | 甲中气球比乙中气球的体积大 | |
| 第③组 | 0.6 g NaHCO3 0.6 g Na2CO3 3 mL 2 mol / L盐酸 | 甲中气球比乙中气球的体积大 | |
| 片刻后,乙中气球又缩小,甲中气球的体积基本不变 | (用离子方程式表示) |
化学活动课上,三组学生分别用图示甲、乙两装置探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查)。
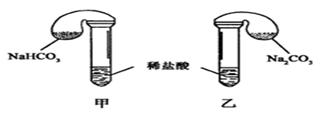
请回答:
(1) 各组反应开始时, 装置中的气球体积先变大,该装置中反应的离子方程式是______。
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格。
| 组 数 | 试剂用量 | 实验现象 (气球体积变化) | 分析原因 |
| ① | 0.42 g NaHCO3;0.53g Na2CO3;3mL4 mol·L-1盐酸 | 甲中气球与乙中气球的体积相等 | 甲、乙盐酸均过量,n(NaHCO3)=n(Na2CO3),ν甲(CO2)=ν乙(CO2) |
| ② | 0.3 g NaHCO3;0.3 g Na2CO3;3mL4 mol·L-1盐酸 | 甲中气球比乙中气球的体积大 | |
| ③ | 0.6 g NaHCO3;0.6 g Na2CO3;3mL 2mol·L-1盐酸 | 甲中气球比乙中气球的体积大 | |
| 片刻后,乙中气球又缩小,甲中气球的体积基本不变 | (用离子方程式表示) |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com